
Специалист по GMP, аудитор фармацевтических предприятий
18 октября в Москве прошла VI Международная конференция «Логистика лекарственных средств. Создавай настоящее из будущего» [1]. Как обычно, на конференции было рассмотрено множество актуальных тем, состоялось объявление итогов очередного общероссийского опроса фармацевтической логистики и качества SCM Pharm Survey, участники получили новый Сборник практических статей GDP Review. Впервые в рамках конференции состоялась отдельная сессия для производителей и дистрибьюторов ветеринарных препаратов — «Основные тенденции в транспортировке и хранении ветеринарной продукции. Маркировка и другие вызовы 2024 года».
Спикерами круглого стола для ветеринарного сектора были начальник отдела организации государственного надзора в сфере обращения лекарственных средств для ветеринарного применения Управления государственного ветеринарного надзора Россельхознадзора Юлия Калинина, руководитель проектов ТГ Фарма ЦРПТ Вильнур Шагиахметов и управляющий директор фармацевтического 3PL-оператора NC Logistic Гарольд Власов. В мероприятии также приняли участие представители таможенных складов и логистических операторов, компаний АВЗ, ГК ВИК, Эланко, Сева Санте Анималь и других.

В начале своей презентации Юлия Калинина представила статистические данные о состоянии рынка ветеринарных препаратов на начало октября 2024 года:
- 93 предприятия осуществляют производство лекарственных средств, при этом 41% российских производителей подтвердили соответствие требованиям Правил надлежащей производственной практики (Good Manufacturing Practice, GMP) ЕАЭС
- 7525 организаций осуществляют фармацевтическую деятельность (в основном это организации розничной торговли)
- Всего зарегистрировано 2367 лекарственных средств, из них 1488 (63%) отечественных и 879 (37%) иностранных.
Отмечается уменьшение объемов ввоза зарубежных вакцин и рост производства отечественных вакцин (зарубежных ввезено 66,7%, отечественных произведено 125,7% от соответствующих объемов ввоза и производства вакцин за весь 2023 год). На начало октября иностранные производители из дружественных и недружественных к России стран суммарно имели 54 действующих заключения о соответствии требованиям Правил GMP ЕАЭС, утвержденных Решением Совета ЕЭК от 03.11.2016 г. № 77 [2].
Спикер напомнила, что с сентября этого года Правила надлежащей дистрибьюторской практики (Good Distribution Practice, GDP) ЕАЭС, утвержденные Решением Совета ЕЭК от 03.11.2016 г. № 80 [3], действуют и в отношении лекарственных средств для ветеринарного применения. В соответствии с п. 15. и п. 16. «Правил регулирования обращения ветеринарных лекарственных средств на таможенной территории ЕАЭС», утвержденных Решением Совета ЕЭК от 21.01.2022 г. № 1 [4]:
- Реализация, транспортировка, хранение и уничтожение ветеринарных лекарственных средств при их обращении на таможенной территории Союза осуществляются в соответствии с Требованиями к реализации, транспортировке, хранению и уничтожению ветеринарных лекарственных средств, являющимися Приложением № 3 к данным Правилам
- Лица, участвующие в дистрибьюции ветеринарных лекарственных средств в соответствии с выполняемыми ими функциями (включая дистрибьюторов и производителей ветеринарных лекарственных средств), независимо от ведомственной принадлежности и формы собственности могут применять требования Правил GDP ЕАЭС, в добровольном порядке.
При этом Статьей 54. Федерального закона от 12.04.2010 г. № 61-ФЗ «Об обращении лекарственных средств» [5] определено, что оптовая торговля лекарственными средствами осуществляется производителями лекарственных средств и организациями оптовой торговли лекарственными средствами по правилам надлежащей дистрибьюторской практики, утвержденным Евразийской экономической комиссией, и правилам хранения лекарственных средств, утвержденным уполномоченным федеральным органом исполнительной власти (в данном случае это Приказ Минсельхоза России от 29.07.2020 г. № 426 «Об утверждении Правил хранения лекарственных средств для ветеринарного применения») [6].

Будут ли учитываться требования Правил GDP ЕАЭС при проведении государственного контроля за соблюдением правил и требований организациями, которые осуществляют оптовую торговлю ветеринарными препаратами?
Юлия Калинина: Безусловно. Эти Правила уже внесены в Приказ Россельхознадзора от 22.12.2020 г. № 1378 [7] — в перечень нормативных правовых актов, содержащих обязательные требования, оценка соблюдения которых осуществляется Россельхознадзором в рамках государственного контроля. Также требования этих Правил планируется внести в Приказ Россельхознадзора от 10 августа 2022 г. № 1198 [8] — в оценочные листы, содержащие список контрольных вопросов.
Насколько сложно для таможенного склада, на котором будут осуществляться нанесение средств идентификации на препараты для ветеринарного применения (маркировка) и, соответственно, их хранение, получить лицензию Россельхознадзора на осуществление фармацевтической деятельности?
Юлия Калинина: Требования к соискателю лицензии на осуществление фармацевтической деятельности в сфере обращения лекарственных средств для ветеринарного применения едины для всех — как для организации оптовой торговли, так для таможенного склада. За последние полтора месяца уже несколько таможенных складов благополучно получили лицензию.
Гарольд Власов: Например, для компании «Эн.Си.Экспресс», являющейся владельцем таможенного склада, этот процесс занял около трех недель.
Вильнур Шагиахметов: Если к середине августа этого года был всего один таможенный склад с лицензией Россельхознадзора на осуществление фармацевтической деятельности с указанием вида работ (услуг) — хранение лекарственных средств для ветеринарного применения, то на текущий момент времени уже пять таможенных складов имеют такую лицензию.
Должен ли таможенный склад, осуществляющий маркировку лекарственных препаратов для ветеринарного применения средствами идентификации, иметь производственную лицензию?
Юлия Калинина: Деятельность по производству лекарственных средств включает в себя работы по перечню согласно приложению № 1 к Постановлению Правительства РФ от 06.07.2012 № 686 «Об утверждении Положения о лицензировании производства лекарственных средств» [9]. В той части, которая касается сферы обращения лекарственных средств для ветеринарного применения, маркировка не входит в этот перечень. Поэтому на сегодняшний день таможенный склад не сможет получить лицензию на производство.
Выступление Вильнура Шагиахметова было связано с Правилами маркировки лекарственных препаратов для ветеринарного применения средствами идентификации, утвержденными Постановлением Правительства РФ № 675 от 27.05.2024 г. [10]. Среди прочего он представил статистические данные по готовности производителей и импортеров ветеринарных препаратов к введению маркировки:
Производители РФ
- 96% производителей, планирующих производство препаратов этом году, оснащены программным обеспечением и оборудованием для маркировки
- 99,5% производимых ветеринарных препаратов с оборудованием и программным обеспечением для маркировки
- 34% производителей уже подают сведения о вводе в оборот в ГИС МТ
Импортеры
- 75% импортеров, планирующих ввоз ветеринарных препаратов на территорию РФ, подтвердили готовность к маркировке
- 93% из объема рынка импортных ветеринарных препаратов оснащены оборудованием для маркировки на иностранных площадках или выбрали таможенный склад
- 21% уже подают сведения о вводе в оборот в ГИС МТ.
Отдельно была представлена актуальная информация по таможенным складам, на которых могут осуществляться нанесение средств идентификации на препараты для ветеринарного применения и, соответственно, их хранение — по регионам, наличию ветеринарного контроля, наличию лицензии от Россельхознадзора на осуществление фармацевтической деятельности и наличию холодильного оборудования.
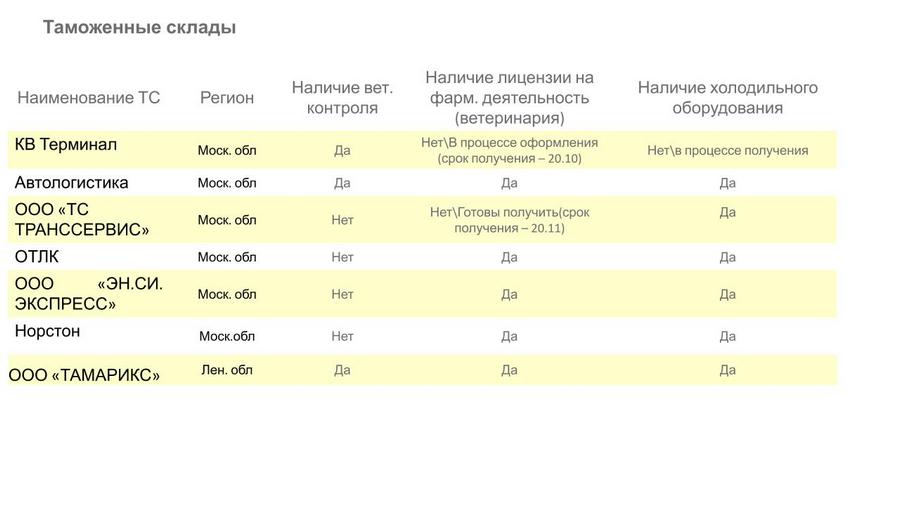
В завершении своего выступления спикер отметил, что по списку импортеров ветеринарных препаратов, который был предоставлен со стороны Россельхознадзора, видно, что этот список пополнился 16 новыми импортерами (в дополнение к 47 уже ранее обозначенным импортерам).
Является ли отсутствие ветеринарного контроля на таможенном складе препятствием к возможности маркировки лекарственных препаратов для ветеринарного применения средствами идентификации?
Вильнур Шагиахметов: Мы долго изучали этот вопрос, рассматривали Приказ Минсельхоза РФ № 542, ФТС РФ № 2013 от 05.11.2009 г. [11]. Мы получили разъяснения в официальном письме от Россельхознадзора, провели встречи с ФТС и получили ответ о возможности маркировки на таможенном складе, имеющем лицензию Россельхознадзора. После прохождения процедуры ветеринарного контроля импортеру достаточно заявить процедуру «Импорт 70» и выполнить перемещение ветеринарных препаратов на любой таможенный склад, который оснащен оборудованием для маркировки и имеет лицензию Россельхознадзора на осуществление фармацевтической деятельности с указанием вида работ (услуг) — хранение лекарственных средств для ветеринарного применения.
Пунктом 3. Постановления Правительства РФ № 675 от 27.05.2024 г. [10] было исключено нанесение средств идентификации на потребительскую упаковку вакцин, имеющих температурный режим хранения и транспортирования минус 60 градусов Цельсия или ниже. Уточните, пожалуйста, с чем связано такое решение?
Вильнур Шагиахметов: У каждой товарной группы, для которой планируется нанесение маркировки, есть свои особенности. Поэтому в процессе проведения эксперимента по маркировке в соответствии с Постановлением Правительства РФ № 2222 от 21.12.2023 г. [12] мы учитывали различные виды и материалы упаковки, на которые необходимо наносить средства идентификации в виде кодов DataMatrix. Некоторые вакцины для птиц в целях обеспечения целостности хранятся в сосуде Дьюара с жидким азотом при температуре -196˚C. В случае маркировки на производственной площадке, с технической точки зрения нет никаких проблем с маркировкой. В том случае, если импортер ветеринарных препаратов выбрал для себя вариант нанесения маркировки на таможенном складе, не так просто определить способ маркировки содержимого сосуда Дьюара (а именно фиксаторов с ампулами), обеспечивающий сохранение эффективности и безопасности вакцины в процессе маркировки. При принятии решения о введении обязательной маркировки Правительство РФ учло в том числе и эти риски, что в свою очередь привело к исключению данной товарной позиции из перечня.
Также на конференции прошло несколько сессий, связанных с GM(D)P, участие в которых могло бы помочь производителям и дистрибьюторам ветеринарных препаратов тщательнее готовиться к внутренним и внешним проверкам.
На всех этапах производства до момента реализации продукция должна находиться на GMP-складе. Нехватка складских площадей — актуальная проблема для фармацевтических производителей, поэтому некоторые производители осуществляют хранение произведенных лекарственных средств на дистрибьютерском складе. Варианты сотрудничества «Фармпроизводитель — Логистического провайдер» разбирались на сессии «Хранение произведенных лекарственных средств на дистрибьютерском складе. Ожидания регулятора», модератором которой была Елена Зелинская, директор по качеству Тульской фармацевтической фабрики.

Жанна Титова, директор по качеству операционной компании «САНТЭНС СЕРВИС», входящей в ГК «Сантэнс», рассказала о возможной модели сотрудничества «GMP-производитель — GDP-провайдер»:
GMP-производитель
- Аренда помещений и оборудования (х/к) для склада фармпроизводителя
- Формирование технического задания по организации склада для хранения
- Открытие обособленного подразделения и принятие в штат персонала склада
- Распространение системы менеджмента качества на новую площадку
- Разработка соглашения по обеспечению качества
GDP-провайдер
- Передача в аренду помещений и оборудования для склада фармпроизводителя
- Организация склада по техническому заданию производителя, включая
- Работы по квалификации/валидации оборудования/помещений
- Имплементация (при необходимости) новых требований заказчика
- Согласование соглашения по обеспечению качества.
Модератором интерактивного образовательного интенсива «Актуальные аспекты внутреннего GDP-аудита на фармацевтических складах» выступила Ирина Спичак, исполнительный директор Евразийской Академии надлежащих практик. Аудитории были предложены три практико-ориентированных кейса. Ответить на некоторые вопросы можно было через микрофон, на другие вопросы — путем выбора правильных ответов в «Телеграм»-канале ЕАНП.

Максим Аблов, руководитель Учебного центра GхP-аудитов ЕАНП подробно рассказал об основных ошибках при самоинспекции склада и способах их устранения. Он отметил, что программа самоинспекции должна быть составлена после оценки деятельности, при понимании процессов, которые осуществляются на складе. Важными элементами проверки фармацевтического склада являются:
- Осмотр всех зон приемки, хранения и отгрузки продукции
- Проверка документации системы качества всех уровней
- Проверка документации, связанной с персоналом
- Проверка документации, связанной с контролем условий хранения
- Проверка документации, связанной с эксплуатацией и обслуживанием оборудования
- Проверка надлежащего функционирования компьютеризированных систем
- Проверка документации по квалификации и валидации
- Проверка данных, связанных с основной деятельностью фармацевтического склада
- Проверка документации по лекарственным средствам, требующим особого обращения
- Транспортировка продукции.
Диалог с экспертом
 Генеральный директор компании RTA Хаким Ибрагимов согласился ответить на несколько вопросов, касающихся прошедшей конференции.
Генеральный директор компании RTA Хаким Ибрагимов согласился ответить на несколько вопросов, касающихся прошедшей конференции.
Хаким, еще раз спасибо за приглашение на очередную конференцию «Логистика лекарственных средств». Когда ответственный за качество в компании RTA Станислав Булыгин выступал от лица организаторов, он отметил, что масштаб конференции уже стал таким, что он не укладывается в одно только понятие «логистика». Как я понимаю, конференция уже вышла на новый уровень?
6 лет нашему проекту — конференции «Логистика лекарственных средств». Год от года конференция развивается. Мы вовлекаем в спираль развития все больше и больше участников, компаний, институций, вместе пробуем разные форматы. И вопросы, которые мы поднимаем, находятся уже за рамками «логистики лекарств». Среди наших делегатов есть представители, связанные с ветеринарными препаратами, медицинскими изделиями, радиофармой и другими направлениями. Мы уже знаковое отраслевое мероприятие. Это развитие происходит в постоянной коммуникации с большим кругом очень разных людей и далеко не всегда из области фармы, что позволяет обогащать наш проект. Была идея переименоваться, так как это уже далеко не только «логистика». Но участники рекомендовали оставить наше название. Так и поступим.
В этом году в рамках конференции впервые успешно прошло отдельное мероприятие для представителей ветеринарного сектора. Каким образом возникла такая идея?
В далеком 1995 году я готовился к поступлению в Армавирский зооветеринарный техникум. Моя мечта была стать ветеринарным врачом, но судьба распорядилась иначе. Но ветеринария всегда в моем сердце. Мы даже проводили большой эфир на канале «Логистика без границ» на тему «Логистика ветеринарной фармацевтики».
А если серьезно, то во всех наших активностях: рабочих группах, онлайн-встречах, сборнике GDP Review, конференциях — всегда принимали участие представители ветеринарного сектора. АВЗ, ГК ВИК, Сева Санте Анималь — активные участники. Мы считаем, что темы нашей конференции актуальны и для компаний этого направления. Тем более, мы сами (RTA) перевозим ветеринарные препараты. Поэтому мы решили провести отдельный круглый стол.
В 2020 году у тебя была идея организовать отдельный «Телеграм»-канал «Логистика ветеринарных препаратов». Канал был создан, но активность участников в нем была низкой. Как ты думаешь, почему?
Мы сосредоточили своим усилия на «Телеграм»-канале «GDP: логистика лекарственных средств» и не стали разделять темы и аудиторию. Мне кажется, пока нет потребности в отдельном канале. Кстати, все материалы прошедшей конференции уже скоро мы откроем на нашем канале (https://t.me/gdpcenter)
Еще с самой первой конференции среди участников были представители регуляторных органов — сначала Росздравнадзора, а теперь и Россельхознадзора. Считаешь ли ты необходимым развивать контакты между регуляторами и бизнес-сообществом?
С 2019 года на наших конференциях всегда присутствуют регуляторы и уполномоченные учреждения: Росздравнадзор, ФНС, ГИЛСиНП, ЦРПТ и другие. Мы считаем крайне важным иметь такой диалог на нашей площадке. Это позволяет аудитории понимать требования и планы государственных органов, а чиновникам — прислушиваться к тому, что интересует бизнес.
В этом году впервые у нас был спикер от Россельхознадзора на отдельном круглом столе, и участники смогли обсудить актуальные вопросы ветеринарной фармацевтики.
Что ждет дальше вашу конференцию?
Развитие и только развитие. Мы провели опрос всех 650 делегатов и получили очень высокие оценки участников. Много поступило идей на 2025 год, новые темы, новые спикеры, новые форматы.
Приглашаем представителей ветеринарного сектора стать авторами журнала GDP Review и спикерами VII конференции «Логистика лекарственных средств». До встречи 17 октября 2025 года!
***
В конце конференции VI конференции «Логистика лекарственных средств» состоялась презентация книги «Женская карьера в качестве». Двадцать женщин, представляющих фармацевтическую индустрию, рассказали свои истории профессионалов от первого лица. На страницах издания показан карьерный путь героинь, представлена история Качества всей фармацевтической индустрии современной России.
Среди авторов книги — директор по качеству компании-производителя ветеринарных препаратов АВЗ Ольга Дубова.

«И конечно самое главное на моем пути — это люди, с которыми я работала и работаю, которые меня окружали и окружают, которых мне посылала судьба и провидение, и без которых я бы никогда не состоялась как профессионал» (из главы «Как стать директором по качеству? Или о хороших людях и не только…»)
| Представленный материал подготовлен с использованием данных, актуальных на 22.10.2024 г. В случае получения новых или дополнительных данных статья может быть обновлена. |
Ссылки:
- SCM Pharm / Мероприятия / VI Международная конференция Логистика лекарственных средств. URL: https://scmpharm.ru/events/6-offline-conf/ (дата обращения 22.10.2024)
- Евразийский экономический союз / Решение Совета Евразийской экономической комиссии от 03.11.2016 г. № 77 «Об утверждении Правил надлежащей производственной практики Евразийского экономического союза». URL: https://docs.eaeunion.org/docs/ru-ru/01411921/cncd_21112016_77 (дата обращения 22.10.2024)
- Евразийский экономический союз / Решение Совета Евразийской экономической комиссии от 03.11.2016 г. № 80 «Об утверждении Правил надлежащей производственной практики Евразийского экономического союза». URL: https://docs.eaeunion.org/docs/ru-ru/01411930/cncd_21112016_80 (дата обращения 22.10.2024)
- КонсультантПлюс / Решение Совета Евразийской экономической комиссии от 21.01.2022 N 1 (ред. от 22.04.2024) «О Правилах регулирования обращения ветеринарных лекарственных средств на таможенной территории Евразийского экономического союза». URL: https://www.consultant.ru/document/cons_doc_LAW_409228/ (дата обращения 22.10.2024)
- КонсультантПлюс / Федеральный закон от 12.04.2010 N 61-ФЗ (ред. от 08.08.2024) «Об обращении лекарственных средств» (с изм. и доп., вступ. в силу с 01.09.2024). URL: https://www.consultant.ru/document/cons_doc_LAW_99350/ (дата обращения 22.10.2024)
- КонсультантПлюс / Приказ Минсельхоза России от 29.07.2020 N 426 «Об утверждении Правил хранения лекарственных средств для ветеринарного применения» (Зарегистрировано в Минюсте России 29.10.2020 N 60648). URL: https://www.consultant.ru/document/cons_doc_LAW_366338/ (дата обращения 22.10.2024)
- КонсультантПлюс / Приказ Россельхознадзора от 22.12.2020 N 1378 (ред. от 07.10.2024) «О перечнях нормативных правовых актов (их отдельных положений), содержащих обязательные требования, оценка соблюдения которых осуществляется Россельхознадзором в рамках государственного контроля (надзора), привлечения к административной ответственности, предоставления лицензий и иных разрешений» (вместе с «Порядком ведения перечней нормативных правовых актов (их отдельных положений), содержащих обязательные требования, оценка соблюдения которых осуществления Россельхознадзором в рамках государственного контроля (надзора), привлечения к административной ответственности, предоставления лицензий и иных разрешений»). URL: https://www.consultant.ru/document/cons_doc_LAW_371944/ (дата обращения 22.10.2024)
- Федеральный портал проектов нормативных правовых актов / О внесении изменений в приказ Федеральной службы по ветеринарному и фитосанитарному надзору от 10 августа 2022 г. № 1198 «Об утверждении формы оценочного листа, содержащего список контрольных вопросов, ответы на которые должны свидетельствовать о соответствии соискателя лицензии, лицензиата лицензионным требованиям, предъявляемым при осуществлении фармацевтической деятельности в сфере обращения лекарственных средств для ветеринарного применения». URL: https://regulation.gov.ru/Regulation/Npa/PublicView?npaID=148600 (дата обращения 22.10.2024)
- КонсультантПлюс / Постановление Правительства РФ от 06.07.2012 N 686 (ред. от 24.01.2024) «Об утверждении Положения о лицензировании производства лекарственных средств». URL: https://www.consultant.ru/document/cons_doc_LAW_132372/ (дата обращения 22.10.2024)
- КонсультантПлюс / Постановление Правительства Российской Федерации от 27.05.2024 № 675 «Об утверждении Правил маркировки лекарственных препаратов для ветеринарного применения средствами идентификации и особенностях внедрения государственной информационной системы мониторинга за оборотом товаров, подлежащих обязательной маркировке средствами идентификации, в отношении лекарственных препаратов для ветеринарного применения». URL: https://www.consultant.ru/document/cons_doc_LAW_477739/ (дата обращения 22.10.2024)
- КонсультантПлюс / Приказ Минсельхоза РФ N 542, ФТС РФ N 2013 от 05.11.2009 (ред. от 19.10.2010) «О ветеринарно-санитарных требованиях к складам временного хранения и таможенным складам» (Зарегистрировано в Минюсте РФ 14.12.2009 N 15579). URL: https://www.consultant.ru/document/cons_doc_LAW_95262/ (дата обращения 22.10.2024)
- КонсультантПлюс / Постановление Правительства РФ от 21.12.2023 N 2222 «О проведении на территории Российской Федерации эксперимента по маркировке средствами идентификации лекарственных препаратов для ветеринарного применения» (вместе с «Положением о проведении на территории Российской Федерации эксперимента по маркировке средствами идентификации лекарственных препаратов для ветеринарного применения»). URL: https://www.consultant.ru/document/cons_doc_LAW_465331/ (дата обращения 22.10.2024)


