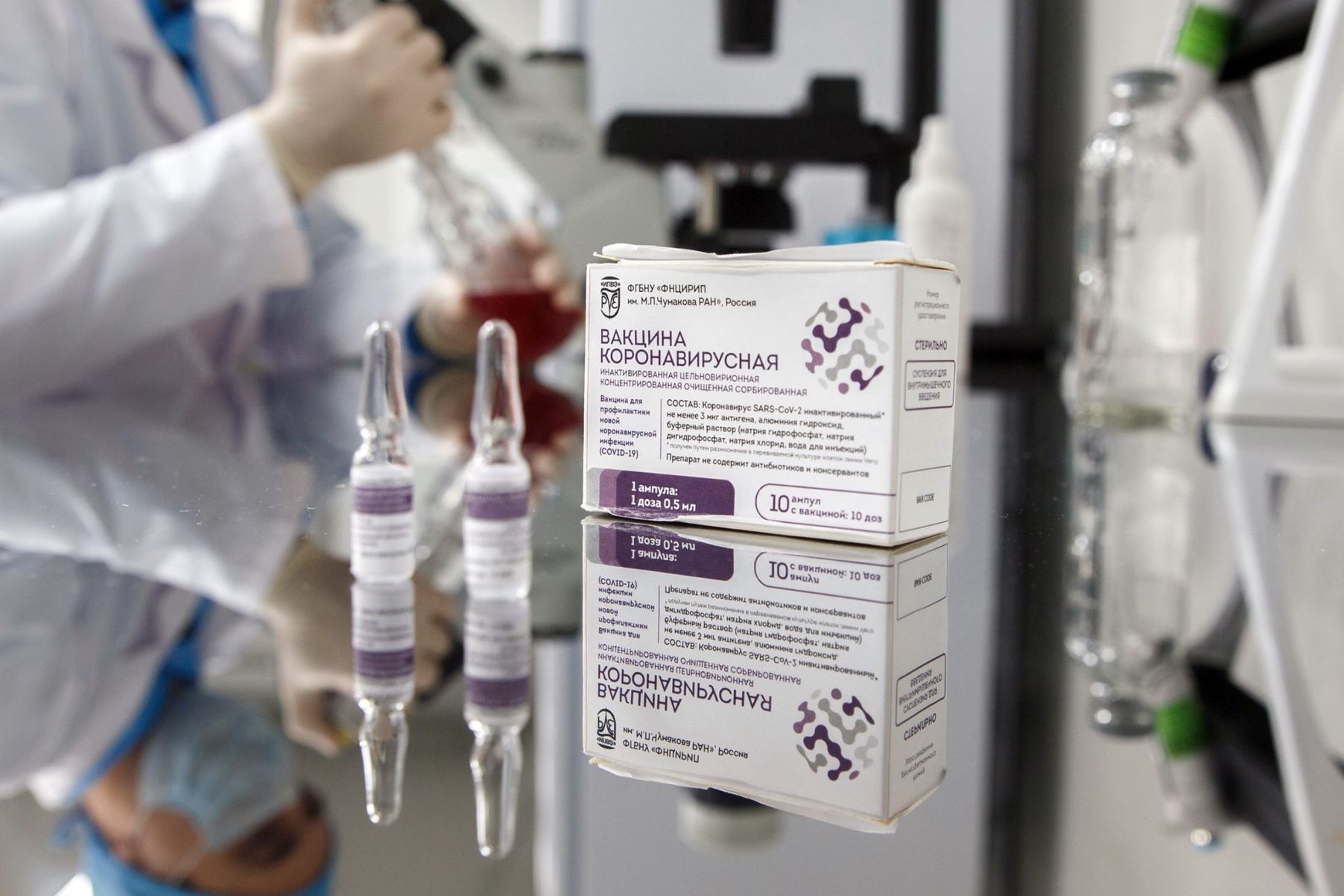
Защитное действие классической инактивированной вакцины, что создана в Федеральном научном центре имени Чумакова (Центр Чумакова), могут проверить на себе 3 тысячи добровольцев уже в феврале-марте 2021 года, об этом рассказал «Российской газете» руководитель иммунологического центра, член-корреспондент РАН Айдар Ишмухаметов.
Сейчас, по его словам, завершается второй этап клинических испытаний и готовятся документы в Минздрав РФ для регистрации новой вакцины против COVID-19.
Что мы получили к середине декабря? Совершенно четкое понимание, что наша вакцина безопасна. Мы провели все необходимые исследования. Сейчас, на втором этапе, можем сказать, что получили понимание об иммунобиологической эффективности, то есть о наличии тех самых антител. Хотя и не считаем это единственным фактором, — заявил генеральный директор центра.
А на уточняющий вопрос, почему в их коллективе не стремились сделать вакцину от коронавируса раньше других, дал такой ответ.
— Хотите знать, почему мы не торопились? Даже при том, что уже с лета технология была нам понятна? Считали необходимым, чтобы к моменту регистрации вакцины у нас был под нее свой производственный участок. И мы такой участок сформировали. Теперь есть отдельный производственный цех, который заработает в феврале… Признаюсь, это не простая работа, когда несколько точек требуется свести в одну. То есть надо было закончить клинические испытания первой и второй фазы. И к этому времени подтянуть готовность площадки — процессы шли параллельно.

Во-вторых, полученные нами бумаги из Всемирной организации здравоохранения уточняют определенные требования к международным тендерам на поставку новых препаратов. Прежде всего, к количеству испытуемых. А поскольку Центр имени Чумакова на сегодняшний день единственный научно-исследовательский институт в России, который по каналам ВОЗ продает свою продукцию, нам крайне важно эту репутацию сохранить…

Если итоги клинических исследований окажутся убедительными, и мы получим регистрационное удостоверение, сразу будем просить Минздрав разрешить участие в третьей, пострегистрационной, фазе. Планируем включить туда около трех тысяч человек. Полагаем, этого достаточно, потому что наша технология более известна, более проверена и понятна.
 Параллельно, как только получим разрешение на регистрацию, сможем уже какое-то количество вакцины запустить в гражданский оборот. И тогда можно будет создавать условия для расширения показаний, в том числе использования вакцины у разных возрастных групп.
Параллельно, как только получим разрешение на регистрацию, сможем уже какое-то количество вакцины запустить в гражданский оборот. И тогда можно будет создавать условия для расширения показаний, в том числе использования вакцины у разных возрастных групп.
Фотографии: Александр Корольков, Российская газета