
Остается всего два месяца до вступления в силу изменений в Федеральный закон от 12.04.2010 г. № 61-ФЗ «Об обращении лекарственных средств», внесенных Федеральным законом от 02.07.2021 г. № 317-ФЗ [1]. С 1 сентября 2023 года ввод в гражданский оборот каждого ввозимого в Российскую Федерацию лекарственного препарата для ветеринарного применения будет осуществляться только при наличии заключения о соответствии производителя лекарственных средств требованиям Правил надлежащей производственной практики (Good Manufacturing Practice, GMP), выданного Россельхознадзором для каждой производственной площадки. В данном обзоре представлена информация по инспектированию производителей ветеринарных препаратов на соответствие требованиям Правил GMP, которое проводят специалисты Федерального государственного бюджетного учреждения «Всероссийский государственный Центр качества и стандартизации лекарственных средств для животных и кормов» (ФГБУ «ВГНКИ»).
Результаты инспектирования
Иностранные производители
Согласно реестру заключений, опубликованному на сайте Россельхознадзора 16.06.2023 г. [2], во втором квартале этого года было выдано 5 заключений о соответствии требованиям Правил GMP. Эти заключения были сделаны в отношении площадок, расположенных в Венгрии, Израиле, Испании и Турции.
Сменилась страна-лидер, в которой было проведено больше всего российских инспекций, по результатам которых за 6 лет инспектирования были приняты решения о выдаче/отказе в выдаче GMP-заключения (28, что составляет 16%) – сейчас это Испания.
В одном из своих выступлений генеральный директор ООО «НВЦ Агроветзащита С-П.» Сергей Енгашев отметил, что в России зарегистрированы ветеринарные препараты из 37 стран. Лидер по импорту лекарств для животных – Испания, компании этой страны поставляют на российский рынок 151 препарат [3].
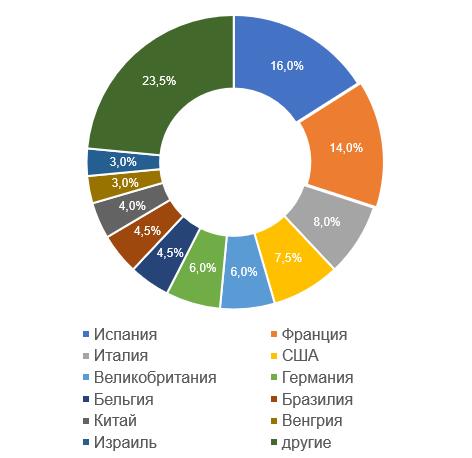
Анализ результатов инспектирования в тех странах, где было проведено наибольшее число российских инспекций, показывает похожие тренды, что и во второй половине прошлого года:
- худшие результаты у производственных площадок, расположенных в США, Бразилии и Германии;
- лучшие результаты у производственных площадок, расположенных в Израиле, а также в Венгрии и Китае.
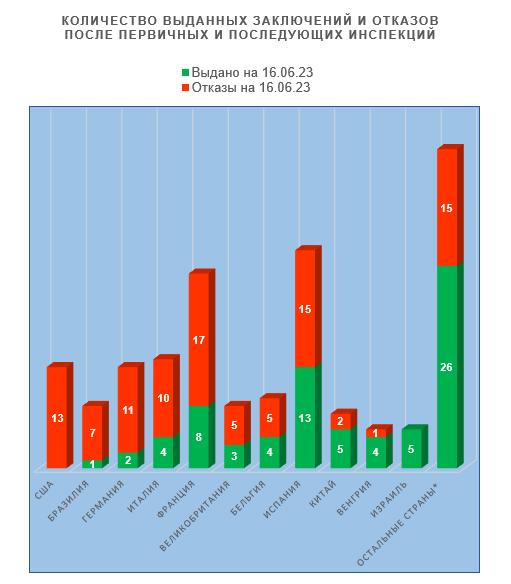
Решений о выдаче/отказе в выдаче GMP-заключения площадкам из США не принималось уже достаточно давно.
Что касается площадок из Бразилии, то в начале июня этого года ФГБУ «ВГНКИ» провело видеоконференцию с представителями бразильского Национального союза производителей товаров для здоровья животных (Sindan). В ходе конференции начальник отдела инспекции ФГБУ «ВГНКИ» Яна Багинская пояснила последовательность действий при подготовке к инспекции, способ подачи заявления и список документов, прилагаемых к нему, требования к производству, а также обратила внимание на выявления несоответствий качества лекарственных средств для ветеринарного применения [4].
По итогам инспекций площадок из Израиля не было ни одного отказа в выдаче заключения.
На сегодняшний день наибольшее число действующих заключений (13) имеют французские, а также испанские и китайские площадки.
Выступая на круглом столе «Открываем двери нашим коллегам из Китая» в рамках выставки «МVC: Зерно-Комбикорма-Ветеринария-2023», исполнительный директор Национальной ветеринарной ассоциации (НВА) Тимур Чибиляев призвал китайских партнеров расширять поставки вспомогательных компонентов и технологий для развития производства ветеринарных препаратов, а также отметил востребованность импорта и локализации в России производства медицинских и ветеринарных лекарственных препаратов китайских компаний [5].
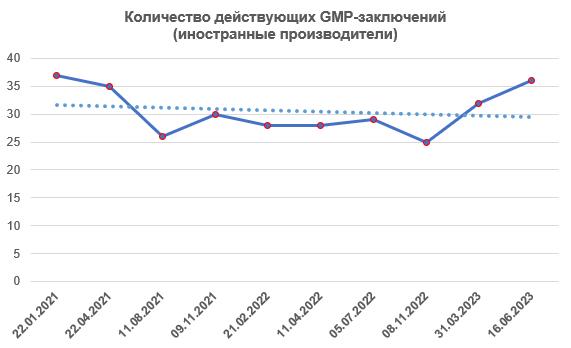
К концу второго квартала количество действующих GMP-заключений немного возросло и достигло примерно такого же уровня, как и в начале 2021 года.
По информации Россельхознадзора, на сегодняшний день зарубежные производители имеют 36 действующих GMP-заключений [6].
Следует иметь в виду, что процесс производства и контроля качества некоторых препаратов может быть распределен между несколькими производственными площадками, которые выполняют отдельные стадии.
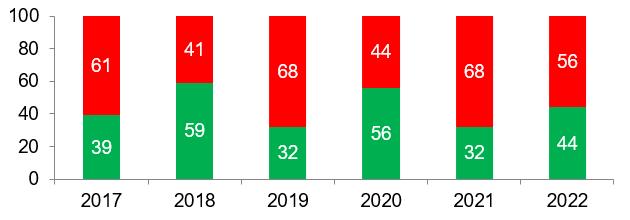
По имеющимся на сегодняшний день данным, в 2022 году процент отказов в выдаче GMP-заключений иностранным производителям был несколько ниже, чем в предыдущем году, при этом средний процент отказов за 6 лет инспектирования составляет 57% (по повторным инспекциям – 65%, по третьим инспекциям – 83%). Такая ситуация не может не беспокоить иностранных производителей ветеринарных препаратов.
Комментарий исполнительного директора ассоциации АВФАРМ Семена Жаворонкова, опубликованный в мае на портале «ЗооМедВет», содержит следующие статистические данные: «С 2017 года на производствах компаний, входящих в АВФАРМ, проведено уже 83 инспекции, включая 28 в online-режиме, по итогам получено 20 сертификатов (из них действуют в этом году всего 8). Результативность составляет <25%» [7].
В апреле этого года информационный портал газеты «Известия» написал [8], что депутаты фракции ЛДПР в Государственной думе направили вице-премьеру РФ Виктории Абрамченко обращение с просьбой отсрочить на два года вступление в силу изменений в Федеральный закон от 12.04.2010 г. № 61-ФЗ «Об обращении лекарственных средств» [1], которые касаются требования о наличии заключения о соответствии производственной площадки иностранного производителя лекарственных средств для ветеринарного применения требованиям Правил GMP ЕАЭС [9].
В соответствии с графиком проведения инспектирования, опубликованном на сайте ВГНКИ 29.06.2023 г. [10], на третий квартал 2023 года запланировано 11 инспекций производителей ветеринарных препаратов, площадки которых расположены в Германии, Индии, Италии, Китае, Нидерландах, Новой Зеландии, США и Франции.
Российские производители
По информации НВА, задачей этого года является сокращение доли импорта в химфармпрепаратах и иммунобиологии. И потенциал у российских производителей, исходя из тенденций развития рынка, существенный: производство вакцин с 2018 года увеличилось в 2,3 раза, гормонов – в 2 раза, а всех категорий ветеринарных средств – на 70% [11].
Согласно реестру на сайте Россельхознадзора [2], во втором квартале текущего года было выдано GMP-заключение производственной площадке ООО «АлексАнн».
На сегодняшний день отечественные производители имеют 29 действующих заключений. При этом по данным директора Департамента ветеринарии Минсельхоза России Марии Новиковой, озвученным во время выставки «МVC: Зерно-Комбикорма-Ветеринария-2023», 100 российских производителей ветеринарных препаратов соответствуют требованиям GMP [12].
В мае этого года новая производственная площадка компании «Ветбиохим», расположенная в особой экономической зоне «Технополис – Москва», получила GMP-сертификат Турции. Сертификат открывает перед компанией новые возможности для развития экспортного потенциала и налаживания торговых связей с представителями дружественных стран [13].
Прошедшие события и мероприятия
Во втором квартале этого года прошло несколько мероприятий, которые могли бы быть полезными производителям для подготовки к инспектированию.
В апреле прошел XXXI Московский международный ветеринарный конгресс MVC 2023.
В рамках конгресса, в секции «Бизнес и Власть» деловой программы мероприятия представила доклад заместитель директора ФГБУ «ВГНКИ» Василина Грицюк. Спикер рассказала о вводе в гражданский оборот лекарственных препаратов для ветеринарного применения, представила полный список документов, регламентирующих данную процедуру, и пояснила порядок выдачи протоколов испытаний [14].
На той же неделе апреля в Москве проходила 22-я выставка «Аналитика Экспо» – крупнейшая в России и странах Восточной Европы Международная выставка лабораторного оборудования и химических реактивов и главное место встречи специалистов в области аналитической химии.
В рамках выставки был организован «Форум для специалистов по контролю качества лекарственных средств», партнером которого выступил Учебный центр ДжиЭксПи.
На форуме были представлены темы: «Обсуждение фармакопеи ЕАЭС», «Как оформить закупку новой единицы оборудования – от идеи до работающего прибора», «Аудит лабораторий контроля качества», «Политика входного контроля на фармацевтическом производстве» [15].

В апреле в Москве состоялся XII Международный фармацевтический форум PharmPRO 2023.
В рамках форума, на специальной сессии «Как обеспечить стабильное производство качественной фармпродукции в условиях постоянных изменений?» были рассмотрены такие ключевые вопросы, как «Работа с поставщиками субстанций при формировании регистрационного досье», «Спецификации по качеству и требования к поставщикам с точки зрения ценности для стабильного производства лекарственных препаратов» и др. [16].

В мае на сайте Минсельхоза России появился раздел «Информация о государственной услуге по аттестации лица, уполномоченного держателем или владельцем регистрационного удостоверения лекарственного препарата для ветеринарного применения», в котором раскрываются подробности об указанной государственной услуге [17].
В соответствии с Приказом Минсельхоза России от 10.11.2022 г. № 795 [18], который вступит в силу с 1 сентября 2023 года, тестовые задания включают в себя пятьдесят вопросов, касающихся требований Правил GMP, а также требований к регистрационному досье на лекарственный препарат для ветеринарного применения.
В представленном на сайте документе «Аттестация лица, уполномоченного держателем или владельцем РУ ЛПВП» представлен перечень нормативных правовых актов, знание которых необходимо для выполнения тестовых заданий и перечень тем вопросов, включенных в тестовые задания [19].
Информации от Департамента ветеринарии о возможности досрочного проведения аттестации на данный момент нет.
Во втором квартале этого года ряд вебинаров был снова посвящен новому Приложению 1 к EU GMP [20], которое будет введено в действие в Европейском Союзе уже со следующего месяца.
Например, компания «ФАРМСТРАТЕГИЯ» провела несколько открытых экспертно-консультационных вебинаров, посвященных новым требованиям к производству стерильных лекарственных средств в свете пересмотра Приложения 1 к EU GMP, в том числе обзору регуляторных нововведений и сложностям их обеспечения, новому в подходах к валидации асептического процесса и др.
В мае на платформе Евразийской академии надлежащих практик состоялся бесплатный вебинар «Валидация стерилизующей фильтрации: современные подходы, регуляторные требования и основные сложности их реализации». Слушатели вебинара смогли получить актуальные сведения об используемых подходах, ознакомиться с текущими трендами и нововведениями в данной области, услышать экспертные мнения касательно обновлений в регуляторных требованиях к валидации процессов стерилизующей фильтрации согласно новой версии Приложения 1 к EU GMP [21].
Вопросы стерилизующей фильтрации часто рассматриваются во время российских инспекций. Например, в прошлом году в «Перечень наиболее часто встречающихся несоответствий при инспектировании производителей лекарственных средств для ветеринарного применения» было включено следующее несоответствие – не подтверждается целостность стерилизующих фильтров через соответствующие интервалы времени [22].
В некоторых международных мероприятиях снова можно было принять участие дистанционно.
В апреле-мае проводились бесплатные видео-встречи «Вопросы-Ответы GMP/GDP» с Александром Александровым, международным экспертом, тренером-консультантом, аудитором группы компаний «ВИАЛЕК». Во время этих встреч у участников была возможность задавать интересующие их вопросы, обсуждать их с коллегами в чате или слушать ответы эксперта на вопросы других участников.
В апреле-июне французская компания Elis провела бесплатные вебинары «Annex 1 Goggles» (организованный совместно с компанией Univet), «How Can You Responsibly Handle End–of–Life Cleanroom Garments?», «Key garment considerations for controlled environments» (организованный совместно с компанией Alsico).
Ближайшие события и мероприятия
В мае открылась регистрация на VIII Всероссийскую GMP-конференцию, которая состоится в Екатеринбурге 26-28 сентября. Организатором конференции выступает Министерство промышленности и торговли Российской Федерации совместно с ФБУ «ГИЛС и НП» [23]. К участию приглашаются представители российских и зарубежных регуляторных органов, производственных площадок, ведущие эксперты отрасли. В течение трех дней конференции пройдет целый ряд тематических сессий и панельных дискуссий, а также традиционные мастер-классы по надлежащим производственным практикам и проведению GMP-инспекций.
Информации о проведении в рамках конференции круглых столов и тематических сессий по ветеринарному направлению на данный момент нет.
В сентябре-октябре на платформе Евразийской академии надлежащих практик пройдет очередной курс повышения квалификации «Подготовка аудиторов производства лекарственных средств» (заочная форма обучения с использованием дистанционных образовательных технологий). По окончании обучения слушателям выдается удостоверение о повышении квалификации установленного образца [24].

20 октября в Москве пройдет V Международная конференция «Логистика лекарственных средств». Регистрация на мероприятие будет открыта 1 августа. В частности, на конференции состоится церемония награждения Премией SCM Pharm 2023. Сообщество руководителей и специалистов по логистике и качеству SCM Pharm готовит издание Сборника практических статей GDP Review 4 [25].
Производителям рекомендуется принимать активное участие в событиях и мероприятиях, связанных с GM(D)P, и тщательнее готовиться к инспектированию.
Представленный материал подготовлен с использованием данных, актуальных на 04.07.2023 г. В случае получения новых или дополнительных данных статья может быть обновлена.
Федеральное государственное бюджетное учреждение «Всероссийский государственный Центр качества и стандартизации лекарственных средств для животных и кормов», ФГБУ «ВГНКИ» – учреждение, уполномоченное на проведение инспектирования производителей лекарственных средств для ветеринарного применения, производство которых осуществляется за пределами Российской Федерации, на соответствие требованиям Правил GMP
Национальная ветеринарная ассоциация, НВА – некоммерческая организация, которая является коллаборации ключевых биофармацевтических компаний
Национальный союз производителей товаров для здоровья животных – Sindicato Nacional da Indústria de Produtos para Saúde Animal, Sindan. Основанный в 1966 году в Бразилии союз объединяет более 90 компаний, на долю которой приходится около 90% бразильского рынка ветеринарных лекарств
Ассоциация ветеринарных фармацевтических производителей АВФАРМ – ассоциация, представляющая на территории Российской Федерации интересы ведущих международных фармацевтических компаний-производителей лекарственных средств для ветеринарного применения (MSD Animal Health, Elanco, Zoetis и Boehringer Ingelheim)
Ссылки:
- Электронный фонд правовых и нормативно-технических документов / Федеральный закон от 02.07.2021 г. № 317-ФЗ «О внесении изменений в Федеральный закон «Об обращении лекарственных средств». URL: https://docs.cntd.ru/document/607142404 (дата обращения 07.2023)
- Россельхознадзор / Деятельность / Госуслуги / Выдача заключения о соответствии производителя (иностранного производителя) лекарственных средств для ветеринарного применения требованиям правил надлежащей производственной практики / Дополнительная информация для заявителя / Государственный реестр заключений о соответствии производителя (иностранного производителя) лекарственных средств для ветеринарного применения требованиям правил надлежащей производственной практики. URL: https://fsvps.gov.ru/ru/gosuslugi/zaklyuchenie-o-sootvetstvii (дата обращения 04.07.2023)
- Ветеринария и жизнь / Зообизнес / Производители призывают продлить ускоренную регистрацию российских ветпрепаратов. URL: https://vetandlife.ru/sobytiya/proizvoditeli-prizyvajut-prodlit-uskorennuju-registraciju-rossijskih-vetpreparatov/ (дата обращения 04.07.2023)
- ФГБУ «ВГНКИ» / Пресс-центр / Новости / Сотрудники ФГБУ «ВГНКИ» приняли участие в видеоконференции с представителями бразильской ассоциации Sindan. URL: https://www.vgnki.ru/sotrudniki-fgbu-vgnki-prinyali-uchastie-v-videokonferencii-s-predstavitelyami-brazilskoj-associacii-sindan.html (дата обращения 04.07.2023)
- Зооинформ / Наращивание импорта ветпрепаратов из Китая прокомментировали в АВФАРМ. URL: https://zooinform.ru/vete/narashhivanie-importa-vetpreparatov-iz-kitaya-prokommentirovali-v-avfarm/ (дата обращения 04.07.2023)
- Ветеринария и жизнь / Зообизнес / Россельхознадзор: 36 иностранных производителей ветпрепаратов прошли GMP-инспекции. URL: https://vetandlife.ru/sobytiya/rosselhoznadzor-36-inostrannyh-proizvoditelej-vetpreparatov-proshli-gmp-inspekcii/ (дата обращения 04.07.2023)
- ЗооМедВет / Статьи / Зарубежные ветеринарные препараты: перспективы в условиях ограничений. URL: https://zoomedvet.ru/?p=10013 (дата обращения 04.07.2023)
- Известия / Рубрики / Экономика / Загнать в укол: в Госдуме увидели риски дефицита препаратов для животных. URL: https://iz.ru/1494625/mariia-perevoshchikova-natalia-bashlykova/zagnat-v-ukol-v-gosdume-uvideli-riski-defitcita-preparatov-dlia-zhivotnykh (дата обращения 07.2023)
- Евразийский экономический союз / Решение Совета Евразийской экономической комиссии от 03.11.2016 г. № 77 «Об утверждении Правил надлежащей производственной практики Евразийского экономического союза». URL: https://docs.eaeunion.org/docs/ru-ru/01411921/cncd_21112016_77 (дата обращения 04.07.2023)
- ФГБУ «ВГНКИ» / Структура / Отдел инспекции производства на соответствие требованиям надлежащей производственной практики / График проведения инспектирования иностранных производителей на соответствие требованиям надлежащей производственной практики. URL: https://www.vgnki.ru/assets/files/2023/grafik-na-sajt-29062023.pdf (дата обращения 04.07.2023)
- Национальная ветеринарная ассоциация / Российский рынок ветеринарной фармацевтики обещает бурный рост. URL: https://rosvet.org/novosti/rossijskij-rynok-veterinarnoj-farmaczevtiki-obeshhaet-burnyj-rost/ (дата обращения 04.07.2023)
- Ветеринария и жизнь / Зообизнес / В Минсельхоз не поступала информация об уходе с рынка иностранных производителей ветпрепаратов. URL: https://vetandlife.ru/sobytiya/v-minselhoz-ne-postupala-informaciya-ob-uhode-s-rynka-inostrannyh-proizvoditelej-vetpreparatov/ (дата обращения 04.07.2023)
- Ветбиохим / Публикации / Сертификат GMP. URL: https://vetbio.ru/public/news-vbh/320/ (дата обращения 04.07.2023)
- ФГБУ «ВГНКИ» / Пресс-центр / Новости / Заместитель директора ФГБУ «ВГНКИ» Василина Грицюк выступила с докладом на Веткогрессе MVC 2023. URL: https://www.vgnki.ru/zamestitel-direktora-fgbu-vgnki-vasilina-gricyuk-vystupila-s-dokladom-na-vetkongresse-mvc-2023.html (дата обращения 04.07.2023)
- Аналитика Экспо / Все мероприятия SMARTLABFORUM 13 апреля. URL: https://analitikaexpo.com/ru/agenda/sessions/SmartLab3/ALL/ (дата обращения 04.07.2023)
- ФармПром.РФ / Материалы партнеров / Как производить качественную фармпродукцию в условиях турбулентности. URL: https://pharmprom.ru/kak-proizvodit-kachestvennuyu-farmprodukciyu-v-usloviyax-turbulentnosti/ (дата обращения 04.07.2023)
- Минсельхоз России / Департамент ветеринарии / Отраслевая информация / Информация о государственной услуге по аттестации лица, уполномоченного держателем или владельцем регистрационного удостоверения лекарственного препарата для ветеринарного применения. URL: https://mcx.gov.ru/ministry/departments/departament-veterinarii/industry-information/ (дата обращения 07.2023)
- Официальный интернет-портал правовой информации / Приказ Министерства сельского хозяйства Российской Федерации от 10.11.2022 № 795 «Об утверждении Порядка аттестации лица, уполномоченного держателем или владельцем регистрационного удостоверения лекарственного препарата для ветеринарного применения». URL: http://publication.pravo.gov.ru/Document/View/0001202211290041 (дата обращения 04.07.2023)
- ФармПром.РФ / Регуляторы фармрынка / Что нужно знать лицу, уполномоченному держателем или владельцем РУ ветпрепарата. URL: https://pharmprom.ru/chto-nuzhno-znat-licu-upolnomochennomu-derzhatelem-ili-vladelcem-ru-vetpreparata/ (дата обращения 04.07.2023)
- The rules governing medicinal products in the European Union – Volume 4 – EU Guidelines for Good Manufacturing Practice for Medicinal Products for Human and Veterinary Use / Annex 1 – Manufacture of Sterile Medicinal Products. URL: https://health.ec.europa.eu/system/files/2022-08/20220825_gmp-an1_enpdf (дата обращения 04.07.2023)
- Евразийская Академия надлежащих практик / Новости и события / 18 мая на платформе Академии состоится бесплатный вебинар на тему валидации процессов стерилизующей фильтрации. URL: https://gxp-academy.org/about/news_and_events/1234/ (дата обращения 04.07.2023)
- ФГБУ «ВГНКИ» / Отдел инспекции производства на соответствие требованиям надлежащей производственной практики / Полезная информация / Перечень наиболее часто встречающихся несоответствий при инспектировании производителей лекарственных средств для ветеринарного применения. URL: https://www.vgnki.ru/otdel-inspekcii-proizvodstva-na-sootvetstvie-trebovaniyam-nadlezhashhej-proizvodstvennoj-praktiki.html (дата обращения 04.07.2023)
- VIII Всероссийская GMP-конференция. URL: http://gosgmp.ru/ (дата обращения 04.07.2023)
- Евразийская Академия надлежащих практик / Образовательная деятельность Образовательные программы (план) / ПК «Подготовка аудиторов производства лекарственных средств». URL: https://gxp-academy.org/education/courses/podgotovka-auditorov-proizvodstva-lekarstvennykh-sredstv-23-2/ (дата обращения 04.07.2023)
- SCM Pharm / Мероприятия / V Международная конференция Логистика лекарственных средств. URL: https://scmpharm.ru/events/5-offline-conf/#terms (дата обращения 04.07.2023)


