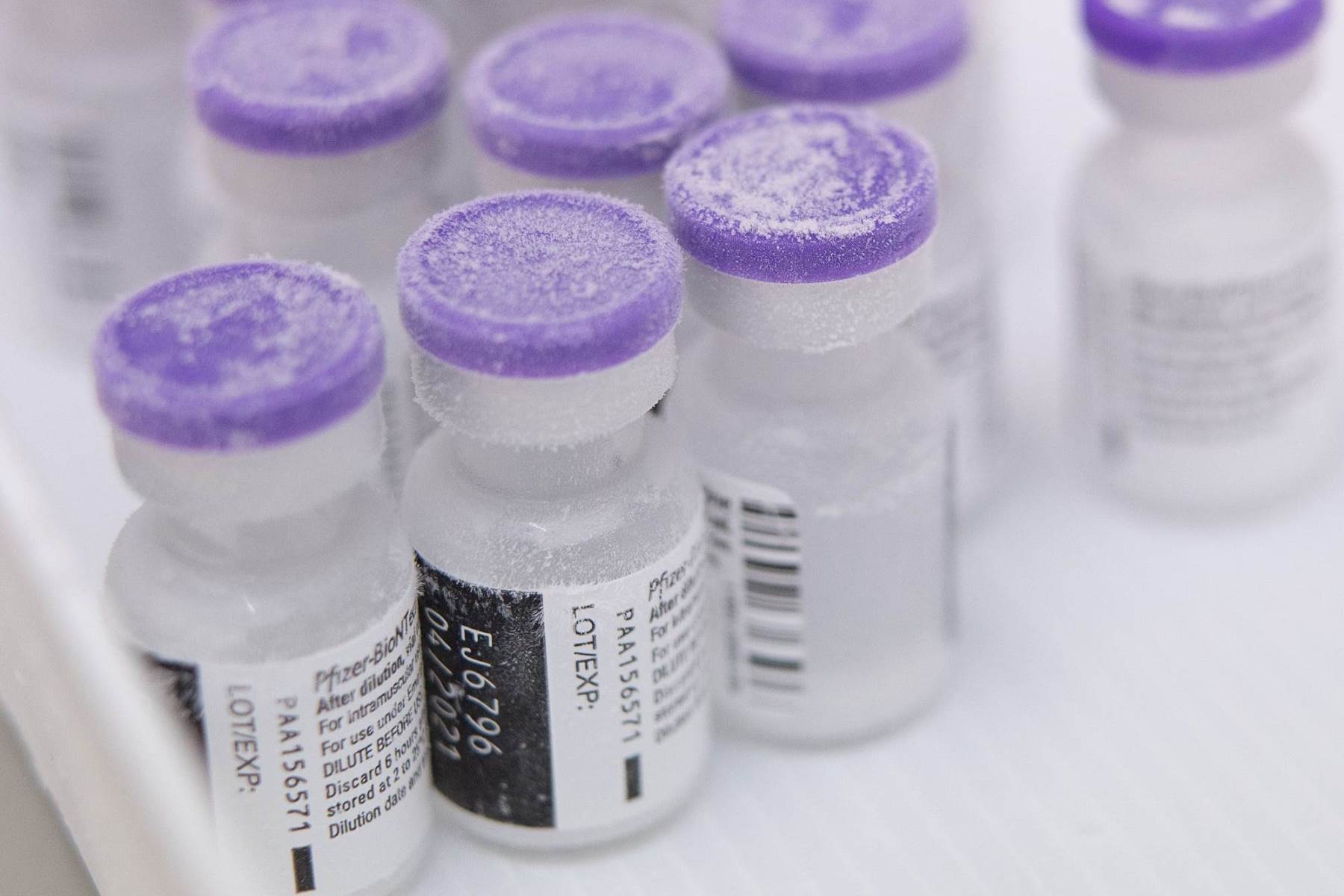
Компании Pfizer Inc и BioNTech SE обратились в Администрацию США по продуктам питания и лекарствам (U.S. Food and Drug Administration — FDA) с просьбой смягчить требования, предъявляемые к вакцине от COVID-19 в отношении хранения её при сверхнизких температурах, что потенциально позволит хранить препарат в морозильных камерах в аптеках, а также упростить логистику вакцины во всем мире.
Фармпроизводители предоставили FDA новые данные о стабильности препарата в качестве поддержки обновления текущей маркировки (и инструкции), что сделает возможным хранение флаконов с противокоронавирусной вакциной при температуре от -15 до -25° C в течение двух недель.
Текущая маркировка мРНК-вакцины предписывает её хранение при температуре от -60 до -80ºC (в течение 6 месяцев), что означает, что вакцина должна быть транспортирована в специально разработанных термических контейнерах, в которых она может находиться в течение 30 дней.
Амеш Адалья (Amesh Adalja), старший научный сотрудник Центра безопасности здоровья Джона Хопкинса (Johns Hopkins Center for Health Security), говорит, что более высокие температуры должны «значительно расширить возможности использования этой вакцины во многих частях мира (или даже в США), которые не имеют возможности для хранения в условиях глубокой заморозки».
FDA подтвердила, что запрос компании Pfizer получен, и изменения, которые запрашивает производитель, должны быть подтверждены данными исследований. Новые данные также будут представлены в мировые регулирующие органы в течение ближайших нескольких недель, сообщили обе компании.
Представленные данные могут облегчить обращение с нашей вакциной в аптеках и предоставить центрам вакцинации еще большую гибкость, — сказал исполнительный директор BioNTech Угур Сахин (Ugur Sahin).
Deutsche Post, которая уже поставила антиковидные вакцины в несколько европейских стран, Израиль, Бахрейн, Мексику, Сингапур и другие государства, заявила, что -25° C будет способствовать некоторому облегчению ситуации, но транспортировка все равно будет делом нелегким. Для авиаперевозок, скорее всего, больше не понадобится сухой лед на борту, что увеличит емкость хранения на каждом самолете.
В компании BioNTech заявили, что они ввели требования по долгосрочному хранению и транспортировке при температуре -70° C из соображений предосторожности, так как компания начала проводить испытания на стабильность и длительность хранения своей вакцины относительно поздно. Несмотря на то, что разработка вакцины была запущена еще в январе 2020 года, параллельно работая над четырьмя соединениями, до июля прошлого года не было принято решение о том, какое из четырех соединений следует разрабатывать дальше, и только после этого начались испытания на стабильность.
ВОЗ также выразила надежду, что смягчение требований к хранению вакцины позволит расширить ее охват.