
В квартальном обзоре представлена информация по инспектированию производителей ветеринарных препаратов на соответствие требованиям Правил надлежащей производственной практики (Good Manufacturing Practice, GMP), которое проводят специалисты Органа инспекции Федерального государственного бюджетного учреждения «Всероссийский государственный Центр качества и стандартизации лекарственных средств для животных и кормов» (ФГБУ «ВГНКИ»).
Результаты инспектирования
Иностранные производители
Согласно реестру заключений, опубликованному на сайте Россельхознадзора 10.03.2025 г. [1], с начала этого года было выдано 3 заключения о соответствии требованиям Правил GMP. Эти заключения были сделаны в отношении площадок, расположенных в Китае, Нидерландах и Хорватии.
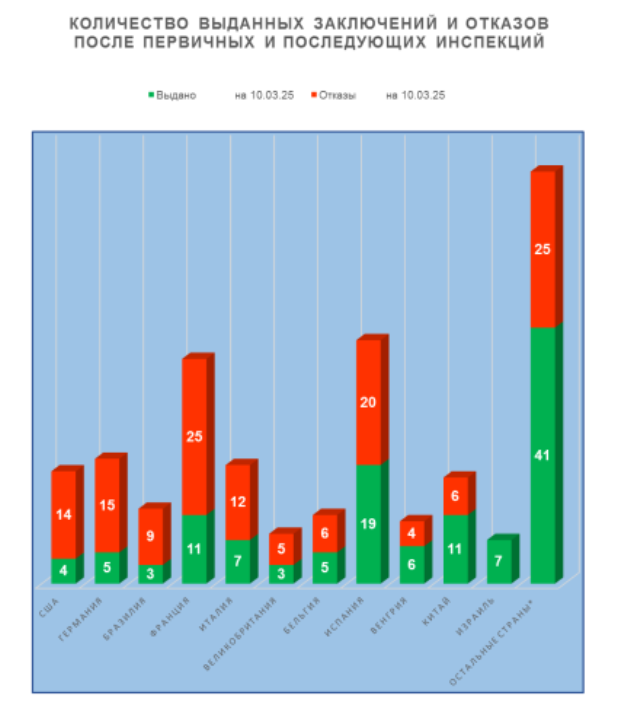
Анализ результатов инспектирования в тех странах, где в 2017-2025 гг. было проведено наибольшее число российских инспекций, показывает следующие тренды:
- худшие результаты у производственных площадок, расположенных в США, Германии и Бразилии, (более 75% отказов в выдаче заключения);
- неплохие результаты у производственных площадок, расположенных в Китае, Венгрии и Испании (не более 51% отказов в выдаче заключения);
- лучшие результаты у производственных площадок, расположенных в Словении, Израиле и Португалии (ни одного отказа в выдаче заключения).
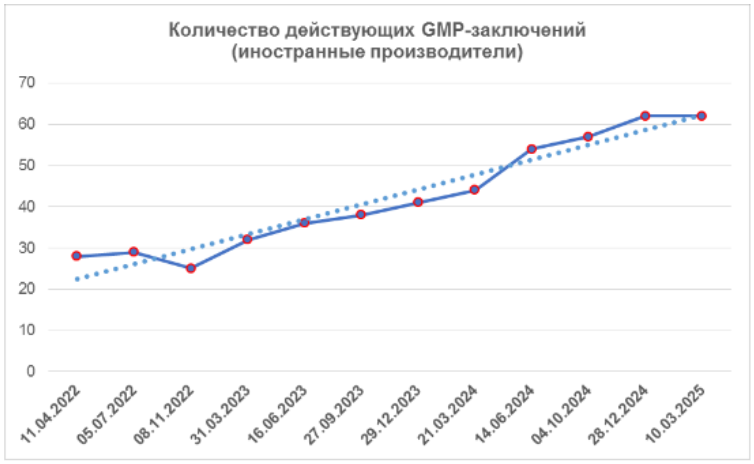
Согласно реестру [1], на сегодняшний день зарубежные производители имеют 62 действующих GMP-заключения.
В рамках прошедшей в марте этого года конференции «PRОЗооРетейл: Правила игры», директор по развитию аналитической компании RNC Pharma Николай Беспалов выступил с презентацией «Розничный рынок ветеринарных препаратов в России. Итоги 2024 г. и перспективы развития в 2025 г.». [2]. Согласно представленным данным, в топ-10 корпораций по объемам продаж на розничном рынке ветпрепаратов в России вошли такие иностранные производители, как Zoetis, Elanco, KRKA, MSD, Boehringer Ingelheim и Bioveta.
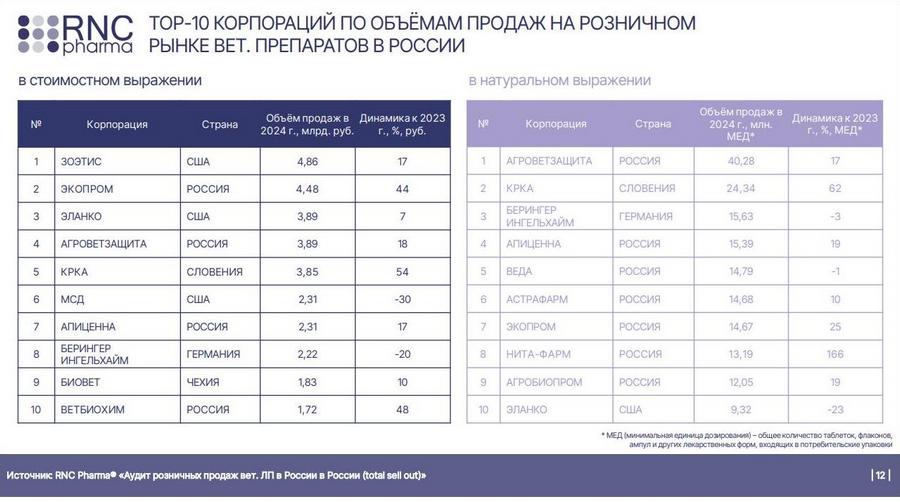
На сегодняшний день производственные площадки и СМО этих зарубежных компаний суммарно имеют более 40% действующих GMP-заключений.
На годовой коллегии Россельхознадзора вице-премьер Дмитрий Патрушев отметил [3], что с 2023 года предусмотрено обязательное наличие GMP сертификата [заключения] для ввода в оборот ветеринарных препаратов: «Добросовестные участники рынка такие сертификаты вовремя получили и продолжают взаимодействие с российскими покупателями».
В соответствии с графиком проведения инспектирования, опубликованном на сайте ВГНКИ 14.03.2025 г. [4], на второй квартал 2025 года запланировано 8 инспекций производителей ветеринарных препаратов, площадки которых расположены в Бразилии, Венгрии, Индии, Испании Китае, Уругвае и Франции.
Российские производители
Согласно реестру на сайте Россельхознадзора [1], GMP-заключения были получены производственными площадками ООО «НИТА-ФАРМ» и АО «Биохимик». На сегодняшний день отечественные производители имеют 33 действующих GMP-заключения.
Все больше компаний-производителей лекарственных средств для медицинского применения стали получать заключение Россельхознадзора о соответствии производителя лекарственных средств для ветеринарного применения требованиям Правил GMP. Например, в 2023-2024 гг. в АО «Биохимик» (производственный комплекс Группы ПРОМОМЕД) была проведена подготовка к началу производства ветеринарных препаратов, включая валидацию производственных линий и выпуск экспериментально-производственных серий четырех лекарственных средств для животных с полным контролем качества. Полученный сертификат [заключение] позволяет ПРОМОМЕД регистрировать ветеринарные препараты по упрощенной процедуре и выводить продукцию на рынок Российской Федерации и стран ЕАЭС [5].
По словам вице-премьера Дмитрия Патрушева [3], Правительство до 2030 года направит 5 млрд. рублей на создание российских ветеринарных препаратов: «Главное для нас — безусловно, укрепление собственных позиций в этой сфере. В рамках нового нацпроекта [«Технологическое обеспечение продовольственной безопасности»] есть отдельное направление по созданию отечественных ветеринарных препаратов».
Прошедшие события и мероприятия
В первом квартале этого года прошло несколько событий и мероприятий, которые могли бы быть интересны производителям, готовящимся к инспектированию.
В феврале Минсельхоз России подготовил проект постановления Правительства РФ «Об определении соответствия производителей лекарственных средств требованиям правил надлежащей производственной практики» [6]. Данным проектом предлагается утвердить Правила, устанавливающие порядок организации и проведения инспектирования производителей лекарственных средств на соответствие требованиям Правил GMP, а также выдачи заключений о соответствии производителя лекарственных средств требованиям Правил GMP. Проектом предусмотрено, что настоящее постановление вступает в силу с 1 сентября 2025 г. и действует до 1 сентября 2031 г. Утратившим силу планируется признать Постановление Правительства РФ от 03.12.2015 г. №1314 [7], регулирующее названные правоотношения в настоящее время.
В том же месяце на площадке Российского союза промышленников и предпринимателей (РСПП) прошла рабочая встреча экспертов для проработки предложений по внесению изменений в «Правила регулирования обращения ветеринарных лекарственных средств на таможенной территории ЕАЭС», утвержденные Решением Совета ЕЭК от 21.01.2022 г. № 1 [8]. К участию в данном мероприятии были приглашены заинтересованные члены Комиссии РСПП по агропромышленному комплексу и продовольственной безопасности, представители отраслевых союзов и ассоциаций, ведущих компаний АПК и федеральных органов исполнительной власти [9].

Многие из представленных экспертам предложений относились к Правилам проведения фармацевтических инспекций, которые являются Приложением №26 к этим Правилам, в частности:
- Привести пункт 5 в соответствие с утвержденной формой сертификата GMP ЕАЭС в Приложении №1 к Правилам: удалить из списка документов, которые подаются в уполномоченный орган для получения сертификата, перечень ветеринарных лекарственных средств, производимых (планируемых к производству) на производственной площадке, так как сертификат выдается на производственные операции и лекарственные формы.
- Дополнить пункт 6: в течение 20 рабочих дней с даты получения соответствующего уведомления заявитель предоставляет недостающие документы, чтобы предоставить заявителю дополнительное время для устранения несоответствий в направленных документах вместо необходимости подачи нового заявления.
- В пункте 15, на уровне ЕАЭС регламентировать предельные сроки процедуры проведения фармацевтической инспекции с момента принятия уполномоченным органом решения о ее проведении: в срок, не превышающий 160 рабочих дней, чтобы избежать затягивания процесса инспектирования и позволить участникам сферы обращения точнее планировать циклы приведения досье в соответствие с требованиями Правил, регистрации, а также подтверждения регистрации ветпрепаратов.
- В пункте 17, увеличить срок направления программы инспектирования инспектируемому субъекту: не позднее чем за 20 рабочих дней до начала проведения инспекции, для улучшения подготовки сторон к инспектированию и оптимизации сроков проведения инспекции.
- В пункте 32, изменить условия выдачи сертификата GMP ЕАЭС: при условии устранения существенных несоответствий в течение срока, обозначенного в CAPA-плане, но не превышающего срок действия сертификата в случае устранения производителем критических несоответствий, либо в случае отсутствия у производителя критических несоответствий (ИЛИ: при условии устранения субъектом в сфере обращения ветеринарных лекарственных средств всех критических несоответствий).
- Дополнить пунктом следующего содержания: возможность проведения инспектирования с использованием средств дистанционного взаимодействия, так как отсутствие такой возможности создает дополнительные сложности при проведении совместных инспекций, предполагающих необходимость синхронизации участия представителей всех государств-членов.
- Дополнить пунктом о возможности выдачи нового сертификата GMP ЕАЭС со сроком окончания действия ранее выданного сертификата, чтобы предоставить возможность актуализации сведений (в части административных изменений, не затрагивающих фактическое место производства) в действующем сертификате без необходимости проведения повторной фармацевтической инспекции.
В конце февраля в пресс-центре медиа группы «Россия сегодня» состоялась пресс-конференция ФГБУ «ВГНКИ» по итогам работы за 2024 год [10]. Результаты инспекционной деятельности представил Cоветник директора ФГБУ «ВГНКИ» Данил Рудняев. Он рассказал об истории формирования системы инспектирования производителей лекарственных средств на соответствие требованиям Правил GMP и подвел итоги проверок, осуществленных в 2024 году: «На сегодняшний день я без лишней скромности могу сказать, что наших инспекторов знают во всем мире, и они пользуются заслуженным уважением».
В марте на базе Евразийской Академии надлежащих практик стартовала первая образовательная программа Практической школы аудиторов. Это образовательная траектория, предназначенная для предоставления специалистам фармацевтических компаний уникальных знаний и компетенций в области аудиторских практик и ключевых аспектов надлежащего функционирования современного фармацевтического предприятия с учетом актуальных требований и рекомендаций нормативно-правовых актов ЕАЭС. В рамках запуска программы состоялся вводный вебинар «Надлежащая лабораторная практика на фармацевтическом предприятии: расследование отклонений от спецификаций и отбор проб исходного сырья» [11].
В конце марта сообщество производителей лекарств и поставщиков PharmPRO провело бесплатный вебинар «Разъяснение требований GMP в отношении упаковочных материалов» [12]. В частности, на данном мероприятии была предоставлена возможность услышать интерпретации требований, относящихся к печатным упаковочным материалам, познакомиться с практикой фармацевтических предприятий, а также получить ответы на вопросы. В своем выступлении международный эксперт Александр Александров особо отметил, что фармпроизводителям стоит сместить акцент с проведения входного контроля печатных упаковочных материалов на проведение аудита поставщиков этих материалов.
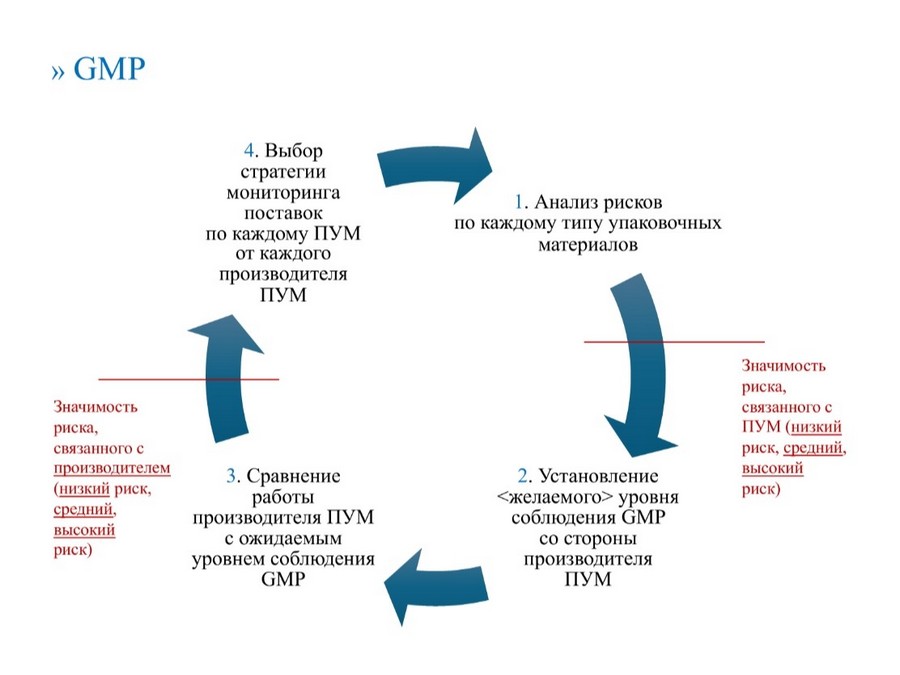
Об упаковочных материалах можно дополнительно прочитать здесь: https://pharmprom.ru/vse-chto-vy-vsegda-xoteli-znat-ob-upakovke-no-boyalis-sprosit-chast-4-upakovochnye-materialy, а про аудит поставщиков печатных вторичных упаковочных материалов можно прочитать здесь: https://pharmprom.ru/audit-postavshhikov-pechatnyx-vtorichnyx-upakovochnyx-materialov/.
В первом квартале фармацевтические инспектора Государственного учреждения «Белорусский государственный ветеринарный центр» (ГУ «БГВЦ») провели инспектирование иностранного производителя ветеринарных лекарственных средств — испанской компании Hipra на соответствие требованиям Правил GMP ЕАЭС [13]. В соответствии с текущим графиком проведения фармацевтических инспекций, опубликованном на сайте ГУ «БГВЦ» [14], на апрель 2025 года запланировано 3 инспекции производителей ветеринарных препаратов, площадки которых расположены в Китае.
Ближайшие события и мероприятия
17 апреля в Москве состоится XIV Международный фармацевтический форум PharmPRO 2025. Это отраслевая площадка для общения и обмена опытом фармкомпаний и участников рынка с целью повышения эффективности работы каждого [15].
В рамках форума будет организовано несколько специальных сессий, в том числе кейс-сессия «От качества процессов к качеству продукции и эффективности производства». На этой сессии запланировано рассмотрение тем: «Как обеспечить производство ресурсами за счет взаимозаменяемости кадров. Опыт внедрения проекта «Мультифункциональность», «Выпуск продукции в срок: как цифровая трансформация ФСК улучшила показатели более чем в 2 раза», «Склад с лицензией Минпромторга. Почему это так важно для организации процессов хранения?» и др.
23-25 апреля в Москве пройдет 23-я Международная выставка «Аналитика Экспо 2025» — единственная в России межотраслевая выставка лабораторного оборудования и химических реактивов [16].
23 апреля в рамках выставки будет организован «Форум специалистов по качеству и регистрации лекарственных средств» при поддержке учебного центра ДжиЭксПи. Среди анонсированных тем: «Регистрационое досье: путеводитель для уполномоченных лиц», «Инспектирование БАД: на стыке ХАССП и GMP».
Производителям рекомендуется принимать активное участие в событиях и мероприятиях, связанных с GM(D)P, и тщательнее готовиться к инспектированию.
| Представленный материал подготовлен с использованием данных, актуальных на 31.03.2025 г. В случае получения новых или дополнительных данных статья может быть обновлена. |
Константин Морозов, специалист по GMP, аудитор фармацевтических предприятий
Федеральное государственное бюджетное учреждение «Всероссийский государственный Центр качества и стандартизации лекарственных средств для животных и кормов», ФГБУ «ВГНКИ» — учреждение, уполномоченное на проведение инспектирования производителей лекарственных средств для ветеринарного применения, производство которых осуществляется за пределами Российской Федерации, на соответствие требованиям Правил GMP
Государственное учреждение «Белорусский государственный ветеринарный центр», ГУ «БГВЦ» — учреждение, уполномоченное Департаментом ветеринарного и продовольственного надзора Министерства сельского хозяйства и продовольствия Республики Беларусь на проведение фармацевтических инспекций производства ветеринарных лекарственных средств на соответствие требованиям Правил GMP
Ссылки:
- Россельхознадзор / Деятельность / Госуслуги / Выдача заключения о соответствии производителя (иностранного производителя) лекарственных средств для ветеринарного применения требованиям правил надлежащей производственной практики / Дополнительная информация для заявителя / Государственный реестр заключений о соответствии производителя (иностранного производителя) лекарственных средств для ветеринарного применения требованиям правил надлежащей производственной практики. URL: https://fsvps.gov.ru/ru/gosuslugi/zaklyuchenie-o-sootvetstvii (дата обращения 31.03.2025)
- RNC Pharma / Новости / Розничный рынок ветеринарных препаратов в России. Итоги 2024 г. и перспективы развития в 2025 г. URL: https://rncph.ru/blog/roznichnyj-rynok-veterinarnyh-preparatov-v-rossii-itogi-2024-g-i-perspektivy-razvitiya-v-2025-g/ (дата обращения 31.03.2025)
- Интерфакс / В России / Правительство до 2030 года направит на создание российских ветпрепаратов 5 млрд рублей. URL: https://www.interfax.ru/russia/1016865 (дата обращения 31.03.2025)
- ФГБУ «ВГНКИ» / Структура / Отдел инспекции производства на соответствие требованиям надлежащей производственной практики / График проведения инспектирования иностранных производителей на соответствие требованиям надлежащей производственной практики. URL: https://www.vgnki.ru/assets/2024/files/grafik-na-sajt-14032025.pdf (дата обращения 31.03.2025)
- ПРОМОМЕД / Новости / «ПРОМОМЕД» получил сертификат соответствия требованиям GMP ЕАЭС при производстве ветеринарной продукции. URL: https://promomed.ru/news/promomed-poluchil-sertifikat-sootvetstviya-trebovaniyam-gmp-eaes-pri-proizvodstve-veterinarnoy-produktsii (дата обращения 31.03.2025)
- Федеральный портал проектов нормативных правовых актов / Проект постановления Правительства Российской Федерации «Об определении соответствия производителей лекарственных средств требованиям правил надлежащей производственной практики». URL: https://regulation.gov.ru/Regulation/Npa/PublicView?npaID=154615 (дата обращения 31.03.2025)
- КонсультантПлюс / Постановление Правительства РФ от 03.12.2015 N 1314 (ред. от 05.09.2020) «Об определении соответствия производителей лекарственных средств требованиям правил надлежащей производственной практики» (вместе с «Правилами организации и проведения инспектирования производителей лекарственных средств на соответствие требованиям правил надлежащей производственной практики, а также выдачи заключений о соответствии производителя лекарственных средств указанным требованиям»). URL: https://www.consultant.ru/document/cons_doc_LAW_190256/ (дата обращения 31.03.2025)
- Евразийский экономический союз / Решение Совета Евразийской экономической комиссии от 21.01.2022 № 1 «О Правилах регулирования обращения ветеринарных лекарственных средств на таможенной территории Евразийского экономического союза. URL: https://docs.eaeunion.org/Pages/DisplayDocument.aspx?s=%7Be1f13d1d-5914-465c-835f-2aa3762eddda%7D&w=9260b414-defe-45cc-88a3-eb5c73238076&l=%7B8a412e96-924f-4b3c-8321-0d5e767e5f91%7D&EntityID=32004 (дата обращения 31.03.2025)
- Фармпром / Репортаж / Эксперты предлагают изменения в правила регулирования ветеринарных лекарств в ЕАЭС. URL: https://pharmprom.ru/eksperty-predlagayut-izmeneniya-v-pravila-regulirovaniya-veterinarnyx-lekarstv-eaes/ (дата обращения 31.03.2025)
- ФГБУ «ВГНКИ» / Пресс-центр / Новости / ФГБУ «ВГНКИ» провело пресс-конференцию по итогам работы за 2024 годи. URL: https://www.vgnki.ru/fgbu-vgnki-provelo-press-konferenciyu-po-itogam-raboty-za-2024-god.html (дата обращения 31.03.2025)
- Евразийская Академия надлежащих практик / Новости / В рамках запуска Практической школы аудиторов состоялся вводный вебинар «Надлежащая лабораторная практика на фармацевтическом предприятии: расследование отклонений от спецификаций и отбор проб исходного сырья». URL: https://gxp-academy.org/about/news_and_events/1863/ (дата обращения 31.03.2025)
- PharmPRO / Мероприятия / Разъяснение требований GMP в отношении упаковочных материалов. URL: https://pharmpro.pro/events/razyasnenie-trebovaniy-gmp-v-otnoshenii-upakovochnykh-materialov/ (дата обращения 31.03.2025)
- Евразийский экономический союз / Решение Совета Евразийской экономической комиссии от 03.11.2016 г. № 77 «Об утверждении Правил надлежащей производственной практики Евразийского экономического союза». URL: https://docs.eaeunion.org/docs/ru-ru/01411921/cncd_21112016_77 (дата обращения 31.03.2025)
- ГУ «БГВЦ» / GMP / План проведения фармацевтических инспекций на 2024-2025 годы / Текущий график проведения фармацевтических инспекций на 2025 год. URL: https://bgvc.by/wp-content/uploads/2025/03/tekushhij-grafik.png (дата обращения 31.03.2025)
- PharmPRO / XIV фармацевтический форум PharmPRO. URL: https://events.pharmpro.pro/forum-2025 (дата обращения 31.03.2025)
- Аналитика Экспо / Деловая программа / Форум специалистов по качеству и регистрации лекарственных средств. URL: https://analitikaexpo.com/ru/agenda/bp_25/SmartLab/Day1-forum/ (дата обращения 31.03.2025)


