
Константин Морозов, специалист по GMP, аудитор фармацевтических предприятий
В соответствии с требованиями Правил надлежащей производственной практики (Good Manufacturing Practice, GMP), перед началом операций по упаковке должны быть предприняты меры, гарантирующие, что рабочая зона, упаковочные линии, печатные машины и другое оборудование являются чистыми и не содержат любые использовавшиеся ранее лекарственные препараты, материалы или документы, если они не требуются для запланированной операции. В этой части статьи мы рассмотрим процедуру проверки чистоты линии (line clearance), которая помогает операторам подготовиться к следующему запланированному процессу и избежать неправильной маркировки, перепутывания и перекрестной контаминации продукции.
В конце прошлого года мне удалось принять участие в Фармацевтическом Форуме Евразийского отделения ISPE в Минске [1], где представители ведущих фармацевтических компаний, регуляторных органов и другие эксперты отрасли обсудили наиболее актуальные вопросы, касающиеся производства лекарственных средств. Одним из запомнившихся мне выступлений была презентация директора по качеству компании «Полисан» Светланы Скорик «Предотвращение перекрестной контаминации как часть требований Глав 3 и 5 GMP ЕАЭС — технические и организационные меры в условиях современного уровня автоматизации». В своей презентации среди общих мер контроля процесса она назвала следующие меры:
- проверка отсутствия в рабочей зоне любых остатков от предыдущих операций (включая документы, любые материалы и пр.);
- QR-кодирование мест обязательной проверки, электронное заполнение «чисто» — сотрудник, как минимум, должен подойти к данному месту — снижение риска неисполнительности;
- идентификация, штрихкодирование, история использования в электронном виде;
- чек-лист проверки внесенных, использованных, оставшихся материалов (в т. ч. инструмента), принцип «хирургического поля».
Давайте попробуем разобраться в том, как некоторые из этих мер могут быть реализованы на практике.
Line clearance vs line cleaning
Для начала предлагаю внимательно прочитать последнее предложение в пункте 5.50 Главы 5 Правил GMP ЕС (EU GMP) [2]: «The line-clearance should be performed according to an appropriate check-list». В Правилах GMP ЕАЭС, утвержденных Решением Совета ЕЭК от 03.11.2016 г. № 77 [3], это предложение звучит так: «Очистку линии следует проводить согласно соответствующей процедуре».
Безусловно, очистку производственного оборудования следует проводить в соответствии с подробными письменными инструкциями (это общее требование изложено в пункте 3.36 Главы 3), но в пункте 5.50 авторы европейского документа имели в виду то, что чистоту линии следует проверять согласно соответствующему чек-листу.
Очистка линии является только одним из этапов line clearance — понятия, которое можно перевести как «чистота линии». Одно из значений слова clearance — «расчистка» используется, когда речь идет об уборке беспорядка, расстановке вещей на свои места, расчистке пространства, выбросе мусора или чего-то ненужного (Кембриджский словарь: clearance — the activity of removing waste or things you do not want from a place). Чек-лист или «контрольный список» обычно представляет собой перечень пунктов, напротив которых ставятся галочки — когда тот или иной пункт будет выполнен, таким образом легко отследить, что и в каком объеме осталось сделать. Line clearance cheks можно перевести как «проверка чистоты линии».
В примечаниях к пункту 1.6 «Packaging equipment and process» меморандума PIC/S PI 028-2 «GMP инспекция, связанная с упаковкой» (GMP inspection related to packaging) [4] понятия line clearance и line cleaning приведены отдельно:
- line clearance — чистота линии (рабочая зона, упаковочные линии, машины для печати этикеток и другое оборудование должны быть чистыми и свободными от любых других ранее использованных продуктов, материалов или документов);
- содержание достаточного уровня детализации в чек-листе по чистоте линии;
- line cleaning — очистка линии.
Из чего состоит процедура line clearance
Еще в первой части статьи говорилось о том, что line clearance — это стандартизированная производственная процедура, обеспечивающая отсутствие на оборудовании и в рабочих зонах продукции, документов и материалов, оставшихся после предыдущего процесса. Эта процедура включает в себя три этапа, которые необходимо соблюдать:
1) line сlearing — это освобождение рабочего пространства линии, т. е. физическое удаление любых материалов от предыдущего процесса упаковки, которые не нужны для следующего процесса упаковки, например, упаковочных материалов, документации, этикеток, форматных частей оборудования, отходов и пр.
2) line сleaning — это очистка, дезинфекция и сушка поверхностей оборудования с целью удаления любых остатков предыдущего продукта перед началом упаковки нового продукта/новой серии продукта. Уровень очистки зависит от того, выполняется ли очистка упаковочной линии между разными сериями одного и того же продукта (частичная очистка) или при смене продукта (полная очистка). В ряде случаев очистке предшествует демонтаж форматных частей, чтобы выполнить очистку более тщательно.
3) line checking — это проверка линии после освобождения рабочего пространства и очистки, которая выполняется перед началом упаковки нового продукта/новой серии продукта. Такая проверка может выполняться оператором(ами) или супервайзером, которые подтверждают, что проверка чистоты линии была выполнена, и подписываются в чек-листе и записи по упаковке серии, с указанием даты и времени проверки. Проверка может также включать в себя контроль температуры и влажности в производственном помещении, калибровку весов и др.
Руководящие документы
В части 211 Раздела 21 Свода федеральных нормативных актов США (Title 21 of the Code of Federal Regulations (CFR), Part 211) [5] понятие line clearance не фигурирует, но в подпункте (6) пункта (b) параграфа 211.67 «Equipment cleaning and maintenance» написано, что письменные процедуры по очистке и техническому обслуживанию оборудования (в том числе принадлежностей, которые используются при производстве, обработке, упаковке или хранении лекарственного средства) среди прочего должны включать в себя проверку чистоты оборудования непосредственно перед использованием. Пункт (с) того же параграфа говорит о том, что записи о техническом обслуживании, очистке, дезинфекции и проверке должны сохраняться.
В документе «Руководство для индустрии: Гонконгское руководство по GMP для вторичной упаковки фармацевтической продукции» (Guidance for Industry: Hong Kong Guide to GMP for the Secondary Packaging of Pharmaceutical Products) [6] понятие line clearance встречается неоднократно. Сначала проверки чистоты линии упоминаются в рекомендациях к пункту 3.7 «Design of the packaging area» как пример правильной организации зоны упаковки: Использование формализованных проверок чистоты линии для каждой упаковочной линии перед началом каждой операции вторичной упаковки, чтобы гарантировать, что в этой зоне нет другого продукта или упаковочного материала, и что эта зона чистая и пригодна для использования. Такая проверка чистоты линии должна быть зафиксирована в записи по упаковке серии.
О line clearance также говорится в рекомендациях к пункту 5.13 «Approval of packaging material supplier» как о требовании к содержанию письменных процедур у поставщиков упаковочных материалов: Процедуры должны включать проверку чистоты линии перед началом печати и содержать инструкции по контролю запуска, повреждений, брака, образцов для контроля качества и излишков отпечатанных материалов.
Наиболее широкое описание процедуры line clearance приведено в рекомендациях к пункту 5.20:
- Проверка чистоты линии должна выполняться до начала каждой операции вторичной упаковки.
- Необходимо провести оценку риска, чтобы определить, какие и где продукты и упаковочные материалы от предыдущих операций могут застрять, упасть или сохраниться. На основании результатов следует составить чек-лист по проверке чистоты линии, которому должны следовать операторы.
- При проведении проверки чистоты линии необходимо строго следовать этому чек-листу, чтобы гарантировать, что все эти места проверены на предмет чистоты перед началом следующей операции.
- Рекомендуется, чтобы проверки чистоты линии выполнялись двумя людьми (один отвечает за проверку, а другой — за перекрестную проверку), и оба должны расписаться в разделе по проверке чистоте линии в записи по упаковке серии.
Здесь же приведен пример: При операциях, связанных с использованием сложного оборудования (такого как конвейерная лента) упаковочные материалы, особенно этикетки, могут застревать между конвейерными лентами. Поэтому ленты необходимо проверять перед каждой новой операцией. Кроме того, проверка чистоты линии является одной из мер предосторожности, которые должны соблюдаться при использовании разрезанных этикеток и нанесении штампов вне линии упаковки (рекомендации к пункту 5.25 «Special care for cut labels and off-line printing»): Это включает дополнительные проверки очистки линии на предмет потерянных печатных материалов, более широкое использование выделенных рабочих зон и составление материального баланса этикеток по завершении упаковки.
Практические примеры
Для того чтобы операторы знали, какие и где продукты и упаковочные материалы от предыдущих операций могут застрять, упасть или сохраниться на линии, можно подготовить фотографии критических мест оборудования и сделать их приложением к СОП по проверке чистоты линии:

Такое приложение к процедуре необходимо периодически пересматривать и, по мере появления информации о новых критических местах оборудования, обновлять фотографии этих мест.
Что касается числа операторов, которые должны заниматься проверкой чистоты линии, то это зависит от организации самой процедуры, например:
- Проверку выполняет один оператор с использованием чек-листа, в котором могут быть указаны критические места оборудования.
- Проверку выполняют два оператора, один из которых проводит осмотр, а второй направляет первого оператора и заполняет чек-лист.
- Проверку выполняет один оператор, следуя порядковым номерам, которые указывают ему путь (специальные стикеры на оборудовании).
- Проверку выполняет один оператор, следуя за нанесенной на полу линией и стикерами на оборудовании, указывающими количество конкретных точек для осмотра:
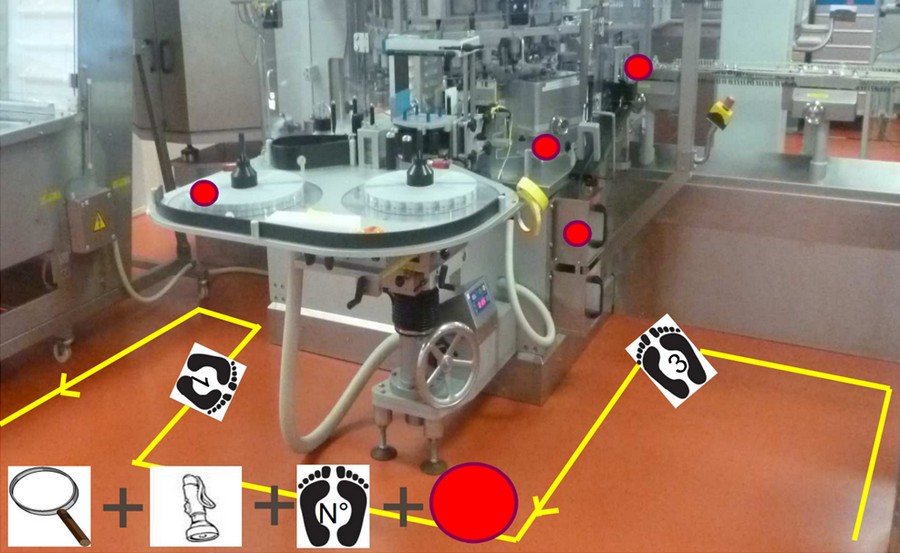
Последний из описанных методов воспроизводит легендарную путеводную «Нить Ариадны» — в данном случае это линия, которая направляет оператора. Преимуществами этого метода являются отказ от бумажного чек-листа и выполнение проверки только одним оператором. При этом я уже обращал внимание на то, что стикеры, которые могут быть использованы для маркировки оборудования, не должны со временем отклеиться и стать источниками контаминации — необходимо следить за их состоянием и при необходимости обновлять. Особенно это касается зоны первичной упаковки. Например, в одном из инспекционных отчетов я видел такое описание несоответствия: «В чистой зоне для маркировки широко используется клейкая лента (скотч). Остатки клея после использования скотча на поверхности оборудования не позволяют его эффективно очищать».
Дэйв Тейлор, менеджер по продукции в компании Catalyx (прежнее название — CXV Global) рассказал автору статьи «Автоматизация чистоты линии» (Automating line clearance) Халли Форчинио [7] и о некоторых других методах проверки: «Некоторые компании разделяют линию на зоны для проверки; другие используют двух операторов. Один оператор начинает с начала линии, а другой — с конца. После встречи в середине каждый оператор продолжает, проверяя работу своего партнера». Это действительно трудоемкий ручной процесс, который зависит от принятия решений человеком, поскольку операторы физически осматривают каждую рабочую зону, упаковочную линию и машину. Некоторые компании даже снимают на видео проверку чистоты линии, но это приводит к многочасовому просмотру и хранению отснятого материала. Эргономика также является проблемой. «Под машинами операторы должны тянуться, сгибаться и разгибаться», — объясняет Дэйв Тейлор. Операторам нередко приходится подниматься по лестницам и выполнять «слепые» проверки области на ощупь, поскольку визуальный осмотр невозможен. В партнерстве с корпорациями в области естественных наук компания Catalyx разработала специальную систему, которая состоит из промышленных камер, установленных в критических местах внутри, над и под машиной/линией:

Эта разработка также включает в себя кабели, процессоры, интерфейс оператора, программное обеспечение и пакет валидационных документов. Система может подключаться к ПЛК (программируемому логическому контроллеру) линии; она оповещает операторов о зонах для проверки и повторно проверяет зону после того, как оператор предпринимает действия. Изображения до и после, которые имеют отметку даты и времени и регистрируются в журнале аудита, являются доказательством того, что чистота линии была проверена должным образом. Систему можно настроить и так, чтобы линия не могла быть перезапущена, пока ПЛК не получит сигнал «готово», указывающий на то, что процесс проверки был успешно завершен.
Чек-листы для проверки
В статье Жасмин Чан «Чистота линии в производстве» (Line сlearance in manufacturing) [8] на сайте компании Tulip Interfaces, приведен пример бумажного чек-листа для проверки чистоты упаковочной линии:
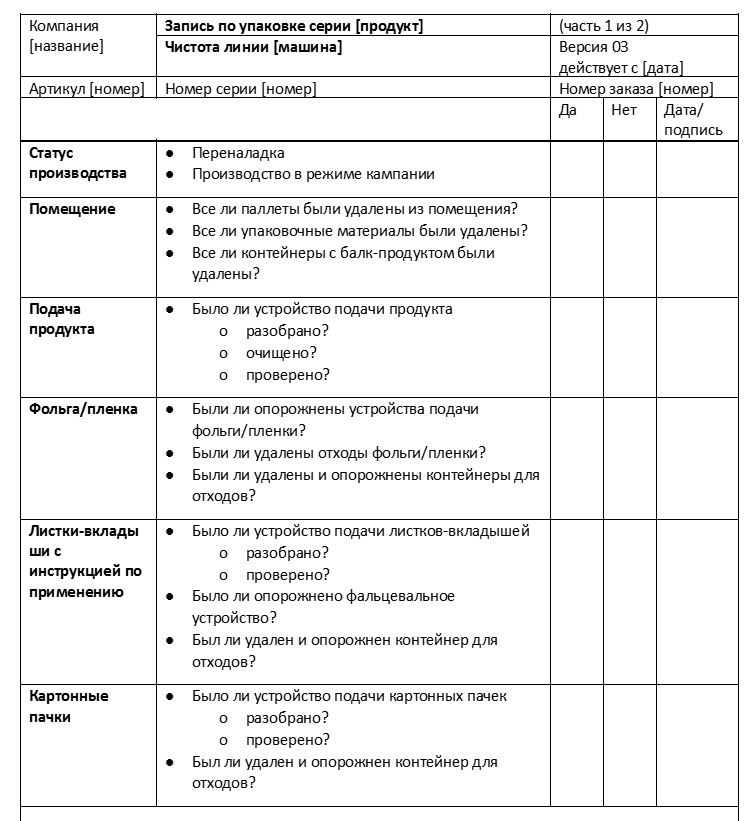
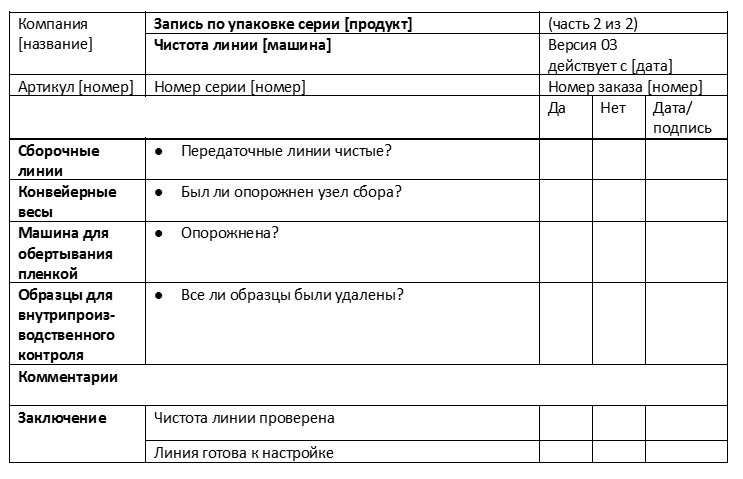
Чек-лист для осмотра критических мест оборудования, где продукты и упаковочные материалы от предыдущих операций могут застрять, упасть или сохраниться, может быть выполнен и в виде схемы, например так:
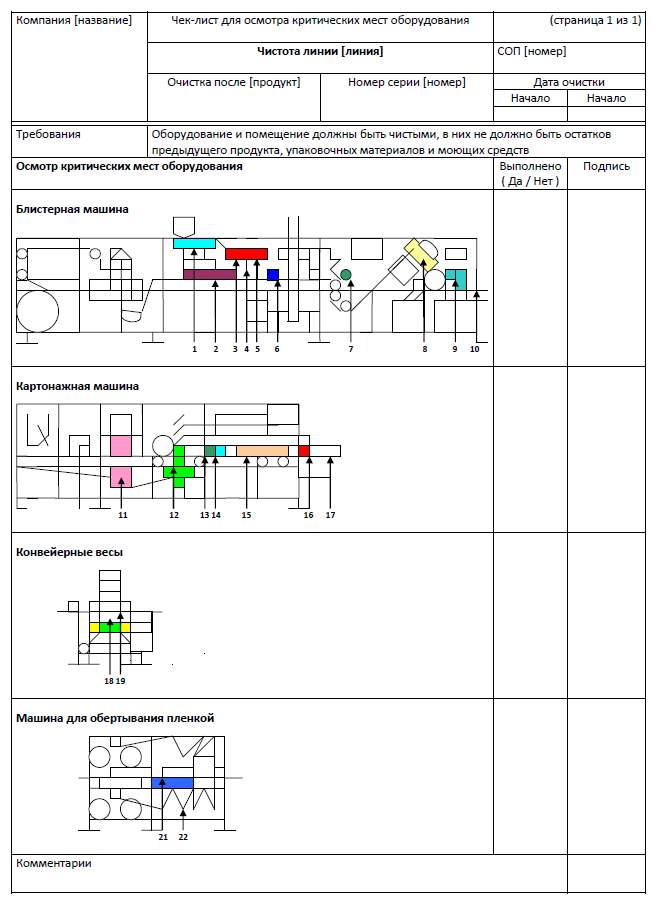
В статье Жасмин Чан также говорится о том, что использование бумажного чек-листа для выполнения и документирования проверки может быть трудоемким и подвержено человеческим ошибкам. Компания Tulip разработала компьютерные приложения по проверке чистоты линии, чтобы гарантировать выполнение необходимых шагов и проверок, отслеживая прогресс и регистрируя завершение проверки в режиме реального времени. Такое приложение можно интегрировать с ERP-системой:
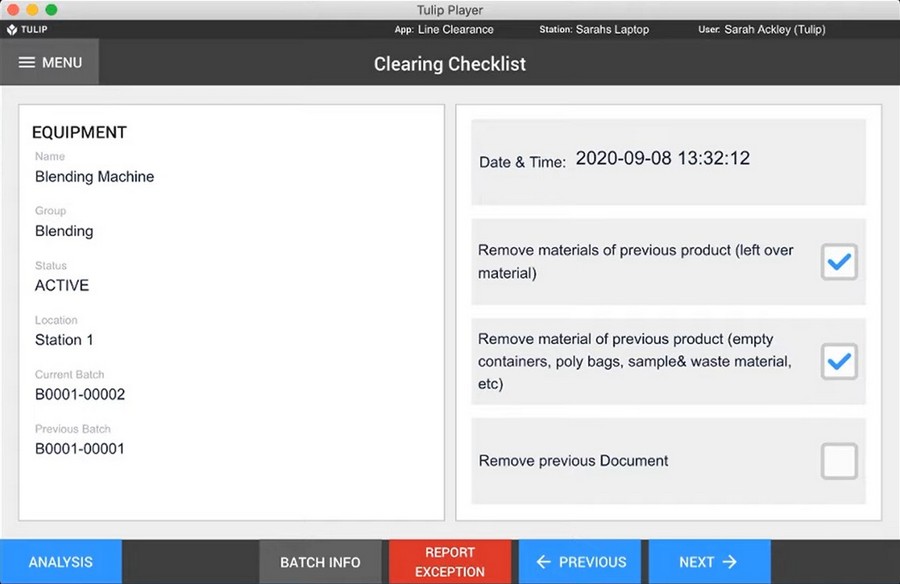
Таким образом, в условиях современного уровня автоматизации, использование IT-решений для контроля выполняемых процессов может привести повышению эффективности работы, снижению риска неисполнительности и улучшению прослеживаемости действий.
Проверка чистоты линии выполняется не только в фармацевтической отрасли, но и в других регулируемых отраслях, таких как производство медицинских изделий, продуктов питания и напитков. Она должна быть частью стандартной рабочей процедуры производителя как мера снижения риска неправильной маркировки, перепутывания и перекрестной контаминации продукции. Для поддержания высокого уровня соответствия и прослеживаемости эта процедура может быть оптимизирована путем ее цифровизации.
| Представленный материал подготовлен с использованием данных, актуальных на 14.02.2025. В случае получения новых или дополнительных данных статья может быть обновлена. |
ССЫЛКИ:
- ISPE ЕАЭС / Новости / От изменений в нормативных документах до выбора IT-решений. О чем говорили на прошедшем в Минске Фармацевтическом Форуме Евразийского отделения ISPE. URL: https://ispe.ru/news/ot-izmenenij-v-normativnyh-dokumentah-do-vybora-it-reshenij-o-chem-govorili-na-proshedshem-v-minske-farmacevticheskom-forume-evrazijskogo-otdeleniya-ispe/ (дата обращения 14.02.2025)
- The rules governing medicinal products in the European Union — Volume 4 — EU Guidelines for Good Manufacturing Practice for Medicinal Products for Human and Veterinary Use / Chapter 5: Production. URL: https://health.ec.europa.eu/document/download/4a1fdb4f-6f6f-49c4-b264-8056e5bbe078_en?filename=chapter_5.pdf (дата обращения 14.02.2025)
- Евразийский экономический союз / Решение Совета Евразийской экономической комиссии от 03.11.2016 г. № 77 «Об утверждении Правил надлежащей производственной практики Евразийского экономического союза». URL: https://docs.eaeunion.org/upload/iblock/bd9/ga9qmu732f3sef7duto3zomhjfpxr0w1/cncd_21112016_77_doc.pdf (дата обращения 14.02.2025)
- Pharmaceutical Inspection Co-operation Scheme / PIC/S GMP Inspection Related to Packaging (PI 028-2). URL: https://picscheme.org/docview/3822 (дата обращения 14.02.2025)
- Code of Federal Regulations (CFR) / Part 211 / Subpart D / § 211.67 Equipment / Equipment cleaning and maintenance. URL: https://www.ecfr.gov/current/title-21/chapter-I/subchapter-C/part-211/subpart-D/section-211.67 (дата обращения 14.02.2025)
- The Drug Office of the Hong Kong Special Administrative Region / Guidance for Industry: Hong Kong Guide to GMP for the Secondary Packaging of Pharmaceutical Products. URL: https://www.drugoffice.gov.hk/eps/do/en/doc/guidelines_forms/Guidance_for_Industry_eng.pdf?v=3r4x4t (дата обращения 14.02.2025)
- PharmTech.com / Automating Line Clearance. URL: https://www.pharmtech.com/view/automating-line-clearance (дата обращения 14.02.2025)
- Tulip Interfaces / Resources / Blog / Line Clearance in Manufacturing. URL: https://tulip.co/blog/line-clearance-in-manufacturing/ (дата обращения 14.02.2025)

